









 Рейтинг: 5.0/5.0 (1805 проголосовавших)
Рейтинг: 5.0/5.0 (1805 проголосовавших)Категория: Инструкции
Чтобы сделать сайт еще более полезным для большого количества пользователей, просим вас оставить ваш отзыв на или ваш личный опыт от применения, ниже в комментариях или на нашем Форуме. спасибо и желаем вам здоровья!
** Ориентировочные оптовые цены в среднем могут существенно или не очень отличаться от цен, представленных в аптеках.Эти цены носят исключительно информативный характер и предназначаются лишь для сравнения ценового диапазона лекарственных препаратов.
* Запатентованные лекарственные препараты могут не иметь дженериков, то есть прямых аналогов с таким же действующим веществом до окончания срока действия патента.
- После момента окончания действия запатентованного препарата, на рынке как правило появляются аналогичные лекарственные средства, имеющие в своем составе схожее действующее вещество, но возможен и другой состав изготовленной лекарственной формы, применение других вспомогательных веществ. Лекарственная форма препаратов может существенно отличаться.
- Некоторые из лекарственных препаратов после окончания периода действия патента не имеют аналогов, вследствие того, что их выпуск просто-напросто нецелесообразен или не возможен по различным причинам. Причины могут быть следующие: регулирование рынка фармацевтики, стратегия фармацевтических производителей, а также фармако-экономические причины.
- Администрация сайта не несет ответственности в случае неправильных выводов, сделанных на основании представленной информации, или если эти данные будут использовать третьими лица с коммерческой целью.
- Администрация сайта не может гарантировать, что видимый терапевтический эффект от использования лекарств-аналогов будет такой же. Перед применением лекарственных препаратов следует обязательно обратиться за консультацией к специалисту с медицинским образованием.
Вспомогательные вещества: натрия кальция эдетат, лактозы моногидрат, крахмал кукурузный, тальк, повидон, магния стеарат.
Состав оболочки: сахароза, повидон, макрогол (полигликоль), кальция карбонат, тальк, воск монтагликолевый.
21 - упаковки ячейковые контурные (1) - коробки картонные.
Клинико-фармакологическая группа: Монофазный пероральный контрацептив
Регистрационные №№:Монофазный комбинированный гестаген-эстрогенный контрацептивный препарат. Индекс Перля: 0.06 на 100 женщин/год (20 000 циклов).
Контрацептивная эффективность достигается тремя дополнительными действиями: подавлением овуляции в гипоталамо-гипофизарной системе, повышением вязкости слизи, что затрудняет проходимость сперматозоидов, снижением восприимчивости эндометрия к имплантации оплодотворенного яйца.
ФармакокинетикаЭтинилэстрадиол быстро и почти полностью всасывается из ЖКТ. Cmax этинилэстрадиола достигается через 1-2 ч. Подвергается эффекту первого прохождения, биодоступность составляет 45%. В плазме этинилэстрадиол связывается с альбумином и с ГСПГ (глобулином, связывающим половые гормоны). T1/2 этинилэстрадиола составляет около 28 ч. Этинилэстрадиол подвергается в печени метаболизму гидроксилацией с образованием метил- и гидроксилметаболитов, глюкоро- и сульфонконъюгатов. 40% производных выводится с мочой и 60% - с фекалиями.
Гестоден быстро и почти полностью всасывается из ЖКТ. Cmax гестодена в плазме достигается через 1-2 ч. Не подвергается воздействию печени во время первого прохождения, биодоступность полная. В плазме связывается с ГСПГ (глобулином, связывающим половые гормоны). T1/2 составляет 18 ч. Подвергается метаболизму путем сокращения цикла А и последующей глюкуронизацией. Около 50% гестодена выводятся с мочой, 33% - с фекалиями.
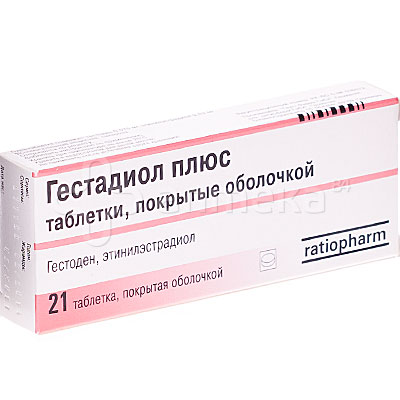
Показания к применению препарата ГЕСТАДИОЛ ПЛЮС— гормональная контрацепция.
Режим дозированияПринимать Гестадиол плюс по 1 таблетки/ в одно и то же время без пропусков в течение 21 дня с последующим 7-дневным перерывом до начала приема следующей упаковки.
Прием Гестадиола плюс начинают в первый день менструации.
При переходе с другого перорального контрацептива
Принять одну таблетку через 7 дней после окончания приема предыдущего контрацептива, содержащего 21 драже. После окончания приема Гестадиола при отсутствии кровотечения в течение 6-7 дней необходимо исключить беременность, прежде чем начать прием следующей упаковки контрацептива.
Случаи пропуска одной или нескольких таблеток
Если пропуск в приеме препарата составляет не более 12 ч. необходимо срочно принять таблетку. Следующую таблетку необходимо принять в установленное время.
Если пропуск в приеме препарата составляет более 12 ч, контрацептивная безопасность не может быть гарантирована. Необходимо срочно принять пропущенную таблетку, даже если в один день будут приняты две таблетки. Далее продолжают курс как обычно, при этом необходимо использовать дополнительные методы контрацепции (презервативы, спермицидные средства) до конца менструального цикла и начала следующей упаковки.
Побочное действиеСо стороны эндокринной системы: часто - снижение либидо; редко - мастодиния, межменструальные кровянистые выделения, олигоменорея, аменорея, изменение либидо; очень редко - аменорея (ановуляторная аменорея у женщин с нерегулярным циклом в анамнезе), аденома гипофиза с пролактинемией (с и без галактореи).
Со стороны половой системы: часто - кандидозный вагинит.
Со стороны пищеварительной системы: часто - тошнота, боли в животе; иногда - изменения аппетита, вздутие живота; очень редко - холелитиаз.
Дерматологические реакции: часто - акне; иногда - хлоазма, гирсутизм, алопеция.
Со стороны сердечно-сосудистой системы: часто - периферические отеки; иногда - артериальная гипертензия; редко - риск тромбоэмболических осложнений (инфаркт миокарда, цереброваскулярные осложнения, флебит, эмболия легочной артерии).
Со стороны ЦНС: часто - депрессия, невроз; иногда - мигрень, вертиго, нарушения зрения.
Со стороны обмена веществ: иногда - гиперлипидемия (гипертриглицеридемия и/или гиперхолестеринемия); редко - нарушенная толерантность к глюкозе.
Со стороны органа зрения: редко - иктеричность склер, непереносимость контактных линз; очень редко - неврит зрительного нерва.
Аллергические реакции: редко - крапивница, ангионевротический отек, анафилактические реакции.
Противопоказания к применению препарата ГЕСТАДИОЛ ПЛЮС— тромбоэмболия артерий в настоящее время или в анамнезе (инфаркт миокарда, цереброваскулярные нарушения);
— тромбоэмболия вен в настоящее время или в анамнезе (флебит, эмболия легочной артерии);
— артериальная гипертензия, коронаропатии, вальвулопатии, нарушения сердечного ритма вследствие тромбообразования;
— метаболические нарушения: сахарный диабет с микро- и макроангиопатией, гиперлипидемии (гипертриглицеридемии, гиперхолестеринемии);
— злокачественные опухоли грудных желез или матки;
— опухоли гипофиза с гиперпролактинемией, галактореей;
— кровотечения из половых путей неясной этиологии;
— непереносимость фруктозы, синдрома плохого усвоения глюкозы и галактозы или дефицита сахарозы-изомальтазы или лактазы;
— тяжелые заболевания печени;
— ожирение (индекс массы тела тела > 30 кг/м 2 );
— нарушения функции почек;
— генитальный герпес;
— период лактации (кормления грудью);
— повышенная чувствительность к активным или вспомогательным веществам препарата.
Применение препарата ГЕСТАДИОЛ ПЛЮС при беременности и кормлении грудьюПротивопоказано применение препарата при беременности и в период лактации.
Особые указанияПеред применением Гестадиола плюс необходимо провести полное медицинское обследование: контроль артериального давления, молочных желез, цервиковагинальной слизи, уровня триглицеридов, холестерина, глюкозы.
С осторожностью и особым вниманием следует назначать препарат пациенткам с эпилепсией, мигренью, бронхиальной астмой, сосудистыми нарушениями в анамнезе, варикозном расширением вен.
Диарея и/или рвота могут уменьшить всасывание гестаген-эстрогенного контрацептива. В этом случае необходимо использовать дополнительно другие методы контрацепции (презервативы, спермициды).
Возможно удлинение продолжительности менструаций в первые месяцы применения Гестадиола плюс . при котором нет необходимости прекращать прием препарата.
В случае если кровотечения продолжаются или появляются впервые после продолжительного срока применения, необходимо выявить возможную органическую причину.
В случае проявления хлоазмы во время беременности или в результате применения гестаген-эстрогенного контрацептива, рекомендуется избегать пребывания на солнце.
До назначения гестаген-эстрогенной контрацепции необходимо исключить риск венозных и артериальных тромбоэмболических осложнений и принять во внимание противопоказания или указания по применению.
При появлении симптомов, свидетельствующих о начавшихся осложнениях, необходимо прекратить прием препарата: сильные и необычные головные боли, нарушение зрения, повышение АД, клинические случаи флебита или эмболии легочной артерии.
Применение любого гестаген-эстрогенного перорального контрацептива увеличивает риск венозного тромбоэмболического осложнения, особенно в течение первого года применения гестаген-эстрогенного перорального контрацептива.
Факторы риска тромбоэмболических венозных осложнений:
— лица, имеющие в анамнезе тромбоэмболические нарушения.
В случае планового хирургического вмешательства необходимо прервать применение гестаген-эстрогенного контрацептива за месяц до планируемой операции.
В случае продолжительной иммобилизации, применение препарата также должно быть прекращено.
В послеродовом периоде возможно использование других методов контрацепции (механических или пероральных гестагенов в микродозах).
В случае венозных тромбоэмболических заболеваний в семье (имевшихся у одного и более членов семьи в возрасте до 50 лет) рекомендуется провести обследование на предмет выявления склонности к венозному тромбозу до начала применения гестаген-эстрогенной контрацепции.
Имеющиеся данные о риске развития инфаркта миокарда не позволяют сделать заключение о разнице уровня риска в группах пациенток, принимавших гестаген-эстрогенные контрацептивы второго и третьего поколения.
Артериальный тромбоэмболический риск, связанный с применением гестаген-эстрогенных контрацептивов возрастает с возрастом и курением, поэтому женщинам старше 35 лет и применяющим гестаген-эстрогенную контрацепцию, особо рекомендуется отказаться от курения.
Другие факторы тромбоэмболического риска:
Артериальный тромботический риск возрастает с возрастом; отношение польза/риск данной контрацепции в возрасте старше 35 лет должно оцениваться в каждом отдельном случае индивидуально.
Гестаген-эстрогенная контрацепция снижает риск развития рака яичников и эндометрия.
Влияние на способность к вождению автотранспорта и управлению механизмами
Может быть нарушена способность к активному участию в дорожном движении.
ПередозировкаСимптомы: тошнота, рвота.
Лечение: промывание желудка и/или назначение активированного угля с последующим восстановлением водно-электролитного баланса.
Лекарственное взаимодействиеВзаимодействия между Гестадиолом плюс и другими компонентами могут привести к увеличению или уменьшению концентрации этинилэстрадиола в плазме. Уменьшение концентрации этинилэстрадиола в плазме может вызвать усиление межменструальных кровотечений и менструальных выделений и возможное снижение контрацептивного действия.
При одновременном применении Гестадиола плюс и:
- индукторов ферментов печени: противосудорожные средства (фенобарбитал, фенитоин, примидон, карбамазепин, топирамат), рифабутин, рифампицин, гризеофувин - снижение концентрации этинилэстрадиола в плазме;
- ритонавира - снижение концентрации этинилэстрадиола в плазме;
- модафинила - снижение концентрации этинилэстрадиола в плазме;
- флунаризина - риск галактореи в связи с вызванным флунаризином повышением чувствительности тканей молочной железы к пролактину;
- тролеандомицина - может повысить риск внутрипеченочного холестаза.
Условия отпуска из аптекПрепарат отпускается по рецепту.
Условия и сроки храненияПрепарат следует хранить в недоступном для детей месте при температуре не выше 25°С. Срок годности - 3 года.
Вспомогательные вещества: натрия кальция эдетат, лактозы моногидрат, крахмал кукурузный, повидон, магния стеарат.
Состав оболочки: сахароза, повидон, полигликоль, кальция карбонат, тальк, воск горный гликолиевый (воск монтангликолевый).
21 шт. - упаковки ячейковые контурные (1) - коробки картонные.
Описание лекарственного препарата ГЕСТАДИОЛ ПЛЮС основано на официально утвержденной инструкции по применению препарата и сделано в 2015 году.
Монофазный комбинированный гестаген-эстрогенный контрацептивный препарат. Индекс Перля: 0.06 на 100 женщин/год (20 000 циклов).
Контрацептивная эффективность обусловлена тремя, дополняющими друг друга, механизмами: подавлением овуляции в гипоталамо-гипофизарной системе, повышением вязкости слизи, что затрудняет проходимость сперматозоидов, снижением восприимчивости эндометрия к имплантации оплодотворенного яйца.
Этинилэстрадиол быстро и почти полностью всасывается из ЖКТ. Cmax этинилэстрадиола достигается через 1-2 ч. Подвергается эффекту "первого прохождения", биодоступность составляет 45%.
В плазме этинилэстрадиол связывается с альбумином и с ГСПГ (глобулином, связывающим половые гормоны).
Этинилэстрадиол подвергается в печени метаболизму путем гидроксилирования с образованием метил- и гидроксилметаболитов, глюкуро- и сульфонконъюгатов.
40% производных выводится с мочой и 60% - с фекалиями. T1/2 этинилэстрадиола составляет около 28 ч.
Гестоден быстро и почти полностью всасывается из ЖКТ. Cmax гестодена в плазме достигается через 1-2 ч. Не подвергается воздействию печени во время "первого прохождения", биодоступность полная.
В плазме связывается с ГСПГ (глобулином, связывающим половые гормоны).
Подвергается метаболизму путем сокращения цикла А и последующей глюкуронизацией.
Около 50% гестодена выводятся с мочой, 33% - с калом. T1/2 составляет 18 ч.
Показания к применению
— гормональная контрацепция.
Гестадиол плюс принимают внутрь по 1 таб./сут в одно и то же время без пропусков в течение 21 дня с последующим 7-дневным перерывом до начала приема следующей упаковки.
Прием Гестадиола плюс начинают в 1 день менструации.
При переходе с другого перорального контрацептива
Принимают 1 таблетку через 7 дней после окончания приема предыдущего контрацептива, содержащего 21 драже. После окончания приема Гестадиола плюс при отсутствии кровотечения в течение 6-7 дней необходимо исключить беременность, прежде чем начать прием следующей упаковки контрацептива.
В случае пропуска одной или нескольких таблеток
Если пропуск в приеме препарата составляет не более 12 ч. необходимо срочно принять таблетку. Следующую таблетку следует принять в установленное время.
Если пропуск в приеме препарата составляет более 12 ч, контрацептивная безопасность не может быть гарантирована. Необходимо срочно принять пропущенную таблетку, даже если в один день будут приняты две таблетки. Далее продолжают курс как обычно, при этом необходимо использовать дополнительные методы контрацепции (презервативы, спермицидные средства) до конца менструального цикла и начала следующей упаковки.
Часто: снижение либидо, депрессия, невроз; тошнота, боли в животе; акне; периферические отеки; кандидозный вагинит.
Иногда: мигрень, вертиго, нарушения зрения; изменения аппетита, вздутие живота; хлоазма, гирсутизм, алопеция; артериальная гипертензия; гиперлипидемия (гипертриглицеридемия и/или гиперхолестеринемия).
Редко: мастодиния, межменструальные кровянистые выделения, олигоменорея, аменорея, изменение либидо; риск тромбоэмболических осложнений (инфаркт миокарда, цереброваскулярные осложнения, флебит, эмболия легочной артерии); нарушение толерантности к глюкозе; иктеричность склер, непереносимость контактных линз; крапивница, ангионевротический отек, анафилактические реакции.
Очень редко: неврит зрительного нерва; аденома гипофиза с пролактинемией (с и без галактореи); холелитиаз; аменорея (ановуляторная аменорея у женщин с нерегулярным циклом в анамнезе).
Противопоказания к применению
— повышенная чувствительность к компонентам препарата;
— тромбоэмболия артерий в настоящее время или в анамнезе (инфаркт миокарда, цереброваскулярные нарушения);
— тромбоэмболия вен в настоящее время или в анамнезе (флебит, эмболия легочной артерии);
— артериальная гипертензия, коронаропатии, вальвулопатии, нарушения сердечного ритма вследствие тромбообразования;
— метаболические нарушения: сахарный диабет с микро- и макроангиопатией, гиперлипидемии (гипертриглицеридемии, гиперхолестеринемии);
— злокачественные опухоли молочной железы;
— злокачественные опухоли матки;
— опухоли гипофиза с гиперпролактинемией, галактореей;
— кровотечения из половых путей неясной этиологии;
— тяжелые заболевания печени;
— ожирение (ИМТ>30 кг/м 2 );
— нарушения функции почек;
— генитальный герпес;
— период лактации (грудного вскармливания);
— непереносимость фруктозы, синдром мальабсорбции глюкозы/галактозы, дефицит сахаразы/изомальтазы или лактазы.
Применение при беременности и кормлении грудью
Противопоказано применение препарата при беременности и в период лактации.
Перед применением Гестадиола плюс необходимо провести полное медицинское обследование: контроль АД, молочных желез, цервиковагинальной слизи, уровня триглицеридов, холестерина, глюкозы.
С осторожностью и особым вниманием следует назначать препарат пациенткам с эпилепсией, мигренью, бронхиальной астмой, сосудистыми нарушениями в анамнезе, варикозном расширением вен.
Диарея и/или рвота могут уменьшить всасывание гестаген-эстрогенного контрацептива. В этом случае необходимо использовать дополнительно другие методы контрацепции (презервативы, спермициды).
Возможно удлинение продолжительности менструаций в первые месяцы применения Гестадиола плюс, при котором нет необходимости прекращать прием препарата.
В случае если кровотечения продолжаются или появляются впервые после продолжительного срока применения, необходимо выявить возможную органическую причину.
В случае проявления хлоазмы при беременности или в результате применения гестаген-эстрогенного контрацептива, рекомендуется избегать пребывания на солнце.
До назначения гестаген-эстрогенной контрацепции необходимо исключить риск венозных и артериальных тромбоэмболических осложнений и принять во внимание противопоказания или указания по применению.
При появлении симптомов, свидетельствующих о начавшихся осложнениях, необходимо прекратить прием препарата: сильные и необычные головные боли, нарушение зрения, повышение АД, клинические случаи флебита или эмболии легочной артерии.
Применение любого гестаген-эстрогенного перорального контрацептива увеличивает риск венозного тромбоэмболического осложнения, особенно в течение первого года применения гестаген-эстрогенного перорального контрацептива.
Факторы риска тромбоэмболических венозных осложнений
Указание в анамнезе на тромбоэмболические нарушения.
В случае планового хирургического вмешательства необходимо прервать применение гестаген-эстрогенного контрацептива за месяц до планируемой операции.
В случае продолжительной иммобилизации, применение препарата также следует прекратить.
В послеродовом периоде возможно использование других методов контрацепции (механических или пероральных гестагенов в микродозах).
В случае венозных тромбоэмболических заболеваний в семье (имевшихся у одного и более членов семьи в возрасте до 50 лет) рекомендуется провести обследование на предмет выявления склонности к венозному тромбозу до начала применения гестаген-эстрогенной контрацепции.
Имеющиеся данные о риске развития инфаркта миокарда не позволяют сделать заключение о разнице уровня риска в группах пациенток, принимавших гестаген-эстрогенные контрацептивы II и III поколения.
Артериальный тромбоэмболический риск, связанный с применением гестаген-эстрогенных контрацептивов возрастает с возрастом и курением, поэтому женщинам старше 35 лет и применяющим гестаген-эстрогенную контрацепцию, особо рекомендуется отказаться от курения.
Другие факторы тромбоэмболического риска
Артериальный тромботический риск возрастает с возрастом. Соотношение польза/риск применения данного препарата в возрасте старше 35 лет следует оценивать в каждом отдельном случае индивидуально.
Гестаген-эстрогенная контрацепция снижает риск развития рака яичников и эндометрия.
Влияние на способность к вождению автотранспорта и управлению механизмами
Может быть нарушена способность к вождению транспортных средств и работе с механизмами.
- плохая переносимость контактных линз
- снижение массы тела
- вагинальные выделения, выделения из молочных желез
- узловатая эритема, мультиформная эритема
- венозные и артериальные тромбоэмболические нарушения**
** - Предполагаемая частота, основанная на данных эпидемиологических исследований группы с применением комбинированных оральных контрацептивов
- «Венозные и артериальные тромбоэмболические нарушения» суммируют следующие заболевания и состояния: окклюзия глубоких периферических вен, тромбоз и эмболия /окклюзия легочных сосудов, тромбоз, эмболия и инфаркт миокарда/инфаркт головного мозга и инсульт не геморрагического характера
Описаниеотдельных побочных реакций.
Побочные реакции с очень низкой частотой или с отсроченным началом развития симптомов, которые рассматриваются как возможно взаимосвязанные с препаратами группы комбинированных оральных контрацептивов, перечислены ниже.
- частота диагноза рака молочной железы слегка повышена среди женщин, принимающих оральные контрацептивы. Поскольку рак молочной железы отмечается редко у женщин младше 40 лет, увеличение числа диагнозов является незначительным по отношению к общему риску развития этого заболевания. Его связь с приемом комбинированных пероральных контрацептивов не доказана
- опухоли печени (доброкачественные и злокачественные).
- женщины с гипертриглицеридемией имеют повышенный риск развития панкреатита при использовании комбинированных оральных контрацептивов
- появление или ухудшение состояний, для которых взаимосвязь с приемом комбинированных пероральных контрацептивов не доказана: желтуха и/или зуд, связанный с холестазом; формирование камней в желчном пузыре; порфирия; системная красная волчанка; гемолитический уремический синдром; хорея Сиденгама; герпес беременных; потеря слуха, связанная с отосклерозом
- у женщин с наследственным ангионевротическим отеком экзогенные эстрогены могут провоцировать или обострять симптомы данного заболевания
- нарушения функции печени
- изменения толерантности к глюкозе или эффекты периферической инсулинорезистентности
- болезнь Крона и неспецифический язвенный колит
Взаимодействия с другими лекарственными препаратами (индукторы ферментов печени, некоторые антибиотики) могут вести к прорывным маточным кровотечениям или снижению контрацептивной надежности препарата (см. раздел «
Лекарственные взаимодействия ПротивопоказанияГестадиол плюс не должен применяться при наличии у женщины какого-либо из состояний, перечисленных ниже. Если какие-либо из этих состояний развиваются впервые на фоне приема, препарат должен быть немедленно отменен:
- гиперчувствительность к любому из компонентов препарата
- беременность или подозрение на нее
- тяжелые заболевания печени, желтуха или стойкий зуд в течение предыдущей беременности, синдром Дабина-Джонсона, синдром Ротора в настоящее время или в анамнезе
- карцинома молочной железы или эндометрия в настоящее время или в анамнезе
- герпес беременных в анамнезе
- ухудшение отосклероза во время беременности
- вагинальное кровотечение неясного генеза
- наличие риска венозной тромбоэмболии (ВТЭ):
· венозная тромбоэмболия - в настоящее время или в анамнезе (тромбоз глубоких вен, тромбоэмболия легочной артерии)
· наследственно обусловленная или приобретенная предрасположенность к венозной тромбоэмболии (например, резистентность к активированному протеину С (включая V фактор Лейдена), дефицит антитромбина III, протеина С или протеина S,
· высокий риск венозной тромбоэмболии из-на наличия множественных факторов риска (см.
Особые указания- наличие или риск артериальной тромбоэмболии (АТЭ):
· артериальная тромбоэмболия в настоящее время или в анамнезе (инфаркт миокарда) или состояния, предшествующие тромбозу (транзиторные ишемические атаки, стенокардия)
· цереброваскулярные нарушения (инсульт) в настоящее время или в анамнезе
· наследственно обусловленная или приобретенная предрасположенность к артериальной тромбоэмболии (гипергомоцистеинемия и антифосфолипидные антитела (антитела к кардиолипину и волчаночный антикоагулянт))
· мигрень с очаговыми неврологическими симптомами в анамнезе
· высокий риск артериальной тромбоэмболии из-на наличия множественных факторов риска (см.
Особые указания• сахарный диабет с сосудистыми осложнениями
• выраженная артериальная гипертензия
• выраженная дислипопротеинемия
- панкреатит с выраженной гипертриглицеридемией в настоящее время или в анамнезе
- опухоли печени (доброкачественные или злокачественные) в настоящее время или в анамнезе
Лекарственные взаимодействияЭффекты других лекарственных средств на Гестадиол плюс
Возможно взаимодействие с лекарственными средствами, индуцирующими ферменты печени, что может способствовать возрастанию клиренса половых гормонов и привести к прорывным кровотечениям и/или снижению контрацептивной эффективности препарата.
Во время приема таких препаратов, женщине следует дополнительно использовать барьерный метод контрацепции в дополнение к Гестадиол плюсу или выбрать другой метод контрацепции. При этом барьерный метод контрацепции следует использовать в течение периода сопутствующего приема препаратов и в течение 28 дней после их отмены. Если период использования барьерного метода предохранения от нежелательной беременности заканчивается позже, чем таблетки в упаковке, нужно переходить к следующей упаковке Гестадиол плюс без обычного перерыва в приеме таблетки.
Вещества, повышающие клиренс половых гормонов (снижающие эффективность комбинированных гормональных контрацептивов вследствие индукции ферментов печени), например:
Ритонавир, карбамазепин, оксикарбазепин, рифампицин, рифабутин, барбитураты, примидон, фенилбутазон, фенитоин, гризеофульвин, топирамат модафинил, фелбамат, гризеофульвин и препараты, содержащие зверобой.
Вещества с различными эффектами на клиренс комбинированных оральных контрацептивов
При сочетанном применении с комбинированными оральными контрацептивами многие ингибиторы ВИЧ/HCV-протеазы и ненуклеозидные ингибиторы обратной транскриптазы могут повышать или снижать концентрацию эстрогенов или прогестинов в плазме крови. Указанные изменения в некоторых случаях могут иметь релевантное значение.
Вещества, снижающие клиренс комбинированных оральных контрацептивов (ингибиторы ферментов)
Аторвастатин, аскорбиновая кислота, парацетамол, конкурентные ингибиторы цитохрома Р450 3A4, такие как противогрибковые препараты (например, итраконазол, вориконазол, флуконазол, индинавир, тролеандомицин, верапамил, макролиды (например, кларитромицин, эритромицин), дилтиазем и грейпфрутовый сок могут повышать концентрацию эстрогена или прогестина или обоих веществ в плазме крови.
Эторикоксиб в дозе от 60 до 120 мг/день повышает концентрацию этинилэстрадиола в плазме в 1,4-1,6 раза при одновременном приеме с комбинированными гормональными контрацептивами, содержащими 0,035 мг этинилэстрадиола.
Влияние комбинированных оральных контрацептивов на другие препараты
Комбинированные оральные контрацептивы могут влиять на метаболизм некоторых других препаратов, что приводит к повышению (например, циклоспорина, теофиллин) или уменьшению (например, ламотриджина) их концентрации в плазме крови и тканях.
В клинических исследованиях назначение гормональных контрацептивов, содержащих этинилэстрадиол, не приводило к какому-либо повышению или хотя бы к слабому повышению концентраций субстрата CYP3A4 (например, мидазолама) в плазме крови, в то время как концентрации субстрата CYP1A2 в плазме крови могут повышаться в слабой степени (например, теофиллина) или в умеренной (например, мелатонина и тизанидина).
Особые указанияМеры предосторожности и предупреждения
Если какие-либо из состояний/факторов риска, указанных ниже, имеются в настоящее время, то следует тщательно взвешивать потенциальный риск и ожидаемую пользу лечения Гестадиол плюсом в каждом индивидуальном случае и обсудить его с женщиной до того, как она решит начать прием препарата. В случае усиления или первого проявления любого из этих состояний или факторов риска необходимо принять решение об отмене препарата.
Риск развития венозной тромбоэмболии (ВТЭ)
Результаты исследований указывают на наличие взаимосвязи между применением комбинированных пероральных контрацептивов и повышенным риском развития венозных и артериальных тромбозов и тромбоэмболических процессов, таких как инфаркт миокарда, тромбоз глубоких вен, тромбоэмболия легочной артерии и цереброваскулярные нарушения. Данные заболевания отмечаются редко.
Риск развития ВТЭ максимален в первый год приема оральных контрацептивов. Повышенный риск присутствует после первоначального использования комбинированных пероральных контрацептивов или возобновления использования одного и того же или разных комбинированных пероральных контрацептивов (после перерыва между приемами препарата в 4 недели и более). Данные крупного клинического исследования с участием 3 групп пациентов показывают, что этот повышенный риск сохраняется преимущественно в течение первых 3 месяцев.
Общий риск венозной тромбоэмболии у пациенток, принимающих пероральные контрацептивы, с низкой дозой эстрогенов (меньше 50 мкг этинилэстрадиола) в 2-3 раза выше, чем у женщин, не использующих их при отсутствии беременности, тем не менее, этот риск остается более низким по сравнению с риском венозной тромбоэмболии при беременности и родах.
Венозная тромбоэмболия может оказаться жизнеугрожающей или привести к летальному исходу в 1-2% случаев.
Венозная тромбоэмболия, проявляющаяся как тромбоз глубоких вен и/или эмболия легочной артерии, может произойти при использовании любых комбинированных пероральных контрацептивов.
У женщин, принимающих комбинированные пероральные контрацептивы, описаны крайне редкие случаи тромбоза других кровеносных сосудов, например печеночных, мезентериальных, почечных, церебральных артерий и вен, а также сосудов сетчатки.
Симптомы тромбоза глубоких вен включают следующее: односторонний отек в ноге или вдоль вены на ноге, боль или дискомфорт в ноге только в вертикальном положении или при ходьбе, локальное повышение температуры в пораженной конечности, покраснение или изменение окраски кожных покровов на ноге.
Симптомы тромбоэмболии легочной артерии заключаются в следующем: внезапное начало необъяснимой одышки или учащенного дыхания, внезапная атака кашля, которая может сопровождаться кровохарканьем, острая боль в грудной клетке, которая может усиливаться при глубоком дыхании, чувство тревоги, сильное головокружение; учащенное или нерегулярное сердцебиение. Некоторые из этих симптомов (например, «одышка» и «кашель») являются неспецифическими и в этой связи могут быть ошибочно интерпретированы как признаки более частых и менее тяжелых нарушений (например, инфекции дыхательных путей).
Артериальная тромбоэмболия может включать в себя цереброваскулярные нарушения, окклюзию сосудов или инфаркт миокарда.
Симптомами цереброваскулярных нарушений могут быть внезапная слабость или онемение лица, верхних и нижних конечностей, особенно с одной стороны тела, внезапная спутанность сознания, нарушение речи или трудности с восприятием; внезапное ухудшение зрения одного или обоих глаз, внезапное нарушение походки, головокружение, потеря равновесия или координации движений, внезапная тяжелая или продолжительная головная боль без видимой причины, потеря сознания или обморок с припадком или без него. Другими признаками окклюзии сосудов могут быть также внезапная боль, отек или слабая синюшность конечностей, симптомы "острого живота".
Симптомы инфаркта миокарда включают: боль, дискомфорт, давление, тяжесть, чувство сжатия или распирания в груди, в руке или за грудиной, чувство дискомфорта с иррадиацией в спину, скулы, гортань, руку, желудок, чувство полноты или распирания в желудке, чувство удушья, холодный пот, тошнота, рвота или головокружение, сильная слабость, чувство тревоги, одышка, учащенное или нерегулярное сердцебиение.
Артериальные тромбоэмболические процессы могут оказаться жизнеугрожающими или привести к летальному исходу.
Следует учитывать вероятность повышенного синергического риска тромбоза у женщин с комбинацией нескольких факторов риска или более высокой выраженностью одного из факторов риска.
В таких случаях повышенный риск может быть выше, чем просто совокупный риск с учетом всех факторов. Гестадиол плюс не следует назначать в случае отрицательной оценки соотношения риск/преимущество (см. раздел «
ПротивопоказанияРиск развития тромбоза (венозного и/или артериального), тромбоэмболических или цереброваскулярных нарушений повышается:
- у курящих (с увеличением количества сигарет или повышением возраста риск в дальнейшем повышается, особенно у женщин старше 35 лет);
- при наличии семейного анамнеза (т.е. венозной или артериальной тромбоэмболии когда-либо у близких родственников или родителей в относительно молодом возрасте), если наследственная предрасположенность известна или предполагается, женщине необходимо проконсультироваться с врачом для решения вопроса о возможности приема комбинированных пероральных контрацептивов;
- при ожирении (индекс массы тела более чем 30 кг/м2);
- при артериальной гипертензии;
- при заболеваниях клапанов сердца;
- при фибрилляции предсердий;
- при длительной иммобилизации, серьезном хирургическом вмешательстве, любой операции на нижних конечностях или обширной травме. В этих ситуациях желательно прекратить использование комбинированных пероральных контрацептивов (в случае планируемой операции, по крайней мере, за четыре недели до нее) и не возобновлять прием в течение двух недель после окончания иммобилизации.
Вопрос о возможной роли варикозного расширения вен и поверхностного тромбофлебита в развитии венозных тромбоэмболий остается спорным. Следует учитывать повышенный риск развития тромбоэмболии в послеродовом периоде.
Циркуляторные нарушения также могут отмечаться при сахарном диабете, системной красной волчанке, гемолитико-уремическом синдроме, хронических воспалительных заболеваниях кишечника (болезнь Крона или неспецифический язвенный колит) и серповидно-клеточной анемии.
Увеличение частоты и тяжести мигрени во время применения комбинированных пероральных контрацептивов (что может предшествовать цереброваскулярным нарушениям) может быть основанием для немедленного прекращения приема этих препаратов.
Биохимические параметры, которые могут быть показателями наследственной или приобретенной предрасположенности к венозному или артериальному тромбозу, включают резистентность к активированному протеину С, гипергомоцистеинемию, дефицит антитромбина-III, дефицит протеина С, дефицит протеина S, антифосфолипидные антитела (антитела к кардиолипину, волчаночный антикоагулянт).
При оценке соотношения риск/преимущество, врачу следует принять во внимание, что адекватное лечение соответствующего состояния может уменьшить связанный с ним риск развития тромбоза. Также следует учитывать, что риск тромбозов и тромбоэмболий при беременности выше, чем при приеме низкодозированных комбинированных пероральных контрацептивов (меньше 0,05 мг этинилэстрадиола).
Наиболее существенным фактором риска развития рака шейки матки является папилломавирусная инфекция (HPV). Имеются сообщения о некотором повышении риска развития рака шейки матки при длительном применении комбинированных пероральных контрацептивов, однако остаются противоречивыми данные о том, в какой степени это может быть связано с другими факторами, в том числе с частотой осмотра шейки матки и особенностями полового поведения, включая использование барьерных методов контрацепции.
Проведенные исследования продемонстрировали, что имеется несколько повышенный относительный риск (RR=1.24) развития рака молочной железы, диагностированного у женщин, которые на момент исследования использовали комбинированные пероральные контрацептивы. Повышенный риск постепенно исчезает в течение 10 лет после прекращения приема этих препаратов. В связи с тем, что рак молочной железы отмечается редко у женщин младше 40 лет, увеличение числа диагнозов рака молочной железы у женщин, принимающих комбинированные пероральные контрацептивы в настоящее время или принимавших недавно, является незначительным по отношению к общему риску развития этого заболевания. Его связь с приемом комбинированных пероральных контрацептивов не доказана. Наблюдаемое повышение риска может быть следствием более ранней диагностики рака молочной железы у женщин, применяющих комбинированные пероральные контрацептивы, биологических эффектов комбинированных пероральных контрацептивов или сочетанием обоих факторов. У женщин, использовавших комбинированные пероральные контрацептивы, выявляется клинически менее выраженный рак молочной железы, чем у женщин, никогда их не применявших.
В редких случаях на фоне применения комбинированных пероральных контрацептивов наблюдалось развитие доброкачественных опухолей печени и еще в более редких случаях развитие злокачественных опухолей печени. В отдельных случаях, опухоли печени могут приводить к жизнеугрожающим интраабдоминальным кровотечениям. В случае появления сильных болей в верхней области живота, увеличения печени или признаков интраабдоминального кровотечения следует учитывать опухоль печени при проведении дифференциального диагноза. Злокачественные опухоли могут быть жизнеугрожающими или привести к летальному исходу.
У женщин с гипертриглицеридемией (или наличия этого состояния в семейном анамнезе) возможно повышение риска развития панкреатита во время приема комбинированных пероральных контрацептивов.
Хотя небольшое повышение артериального давления было описано у многих женщин, принимающих комбинированные пероральные контрацептивы, клинически значимые повышения отмечались редко. Тем не менее, если во время приема комбинированных пероральных контрацептивов развивается стойкое, клинически значимое повышение артериального давления, следует отменить эти препараты и начать лечение артериальной гипертензии. Прием комбинированных пероральных контрацептивов может быть продолжен, если с помощью гипотензивной терапии достигнуты нормальные значения артериального давления.
Следующие состояния, наблюдаемые при беременности, могут также появляться или ухудшаться при приеме комбинированных пероральных контрацептивов: желтуха и/или зуд, связанный с холестазом; порфирия; системная красная волчанка; гемолитический уремический синдром; хорея Сиденгама; герпес беременных; потеря слуха, связанная с отосклерозом. Однако взаимосвязь между развитием указанных состояний и приемом комбинированных пероральных контрацептивов не доказана.
У женщин с наследственным ангионевротическим отеком экзогенные эстрогены могут провоцировать или обострять симптомы данного заболевания.
При наличии острых или хронических нарушений функции печени необходимо решить вопрос прекращения использования комбинированных пероральных контрацептивов, до тех пор, пока показатели функции печени не вернутся в норму. При развитии рецидивирующей холестатической желтухи, которая развивается впервые во время беременности или предыдущего приема половых гормонов следует прекратить прием комбинированных пероральных контрацептивов.
Хотя комбинированные пероральные контрацептивы могут оказывать влияние на резистентность к инсулину и толерантность к глюкозе, нет необходимости изменения терапевтического режима у больных сахарным диабетом, использующих низкодозированные комбинированные пероральные контрацептивы (<0,05 мг этинилэстрадиола). Тем не менее, женщины с сахарным диабетом должны тщательно наблюдаться во время приема комбинированных пероральных контрацептивов.
На фоне применения комбинированных пероральных контрацептивов наблюдались проявления повреждения сосудов сетчатки глаза, отек диска зрительного нерва; формирование камней в желчном пузыре; гиперинсулинизм; гипертриглицеридемия; снижение ЛПВП; болезни Крона и неспецифического язвенного колита.
Женщины со склонностью к хлоазме во время приема комбинированных пероральных контрацептивов должны избегать длительного пребывания на солнце и воздействия ультрафиолетового излучения.
В одном таблетки препарата Гестадиол плюс содержится 35 мг лактозы.
У пациенток с редкими наследственными нарушениями, такими как непереносимость галактозы, дефицит лактазы Lapp или глюкозо-галактозная мальабсорбция, находящихся на безлактозной диете, следует учитывать количество лактозы, содержащейся в Гестадиол плюсе.
Прием комбинированных пероральных контрацептивов может влиять на результаты некоторых лабораторных тестов, включая показатели функции печени, почек, щитовидной железы, надпочечников, уровень транспортных белков в плазме, показатели углеводного обмена, параметры коагуляции и фибринолиза. Изменения обычно не выходят за границы нормальных значений.
Перед началом применения препарата, а также периодически в процессе применения препарата женщине рекомендуется пройти тщательное общемедицинское и гинекологическое обследование (включая измерение артериального давления, исследование молочных желез, органов брюшной полости и малого таза, в том числе цитологическое исследование цервикальной слизи), исключить беременность. Важно проводить периодические медицинские обследования, поскольку противопоказания (например, транзиторные ишемические атаки и другие) или факторы риска (например, наследственная предрасположенность к венозным или артериальным тромбозам) могут проявиться в процессе применения препарата.
Следует предупредить женщину, что препараты типаГестадиол плюсане предохраняют от ВИЧ-инфекции (СПИД) и других заболеваний, передающихся половым путем!
Эффективность комбинированных пероральных контрацептивных препаратов может быть снижена при пропуске таблетки, при рвоте и диарее или в результате лекарственного взаимодействия.
Влияние на менструальный цикл
На фоне приема комбинированных пероральных контрацептивов могут отмечаться нерегулярные кровотечения (мажущие кровянистые выделения или прорывные кровотечения), особенно в течение первых месяцев применения. Поэтому, оценка любых нерегулярных кровотечений должна проводиться только после периода адаптации, составляющего приблизительно три цикла. Если нерегулярные кровотечения повторяются или развиваются после предшествующих регулярных циклов, следует провести тщательное обследование для исключения злокачественных новообразований или беременности.
У некоторых женщин во время перерыва в приеме таблетки может не развиться кровотечение отмены. Если комбинированные пероральные контрацептивы принимались согласно указаниям, маловероятно, что женщина беременна. Тем не менее, если до этого комбинированные пероральные контрацептивы принимались нерегулярно или, если отсутствуют подряд два кровотечения отмены, до продолжения приема препарата должна быть исключена беременность.
Применение у детей и подростков
Гестадиол плюс следует применять только после наступления менструаций.
Беременность и период лактации
Гестадиол плюс не назначается во время беременности. Если во время приема препарата выявляется беременность, необходимо сразу же отменить его прием. Однако обширные эпидемиологические исследования не выявили никакого повышенного риска дефектов развития у детей, рожденных женщинами, получавшими комбинированные пероральные контрацептивы до беременности или тератогенного действия, когда комбинированные пероральные контрацептивы принимались по неосторожности в ранние сроки беременности.
Прием комбинированных пероральных контрацептивов может уменьшать количество грудного молока и изменять его состав, поэтому, их использование в целом не рекомендуется до прекращения грудного вскармливания. Небольшое количество половых стероидов и/или их метаболитов может выводиться с молоком.
Особенности влияния лекарственного средства на способность управлять автотранспортом и потенциально опасными механизмами.
Не наблюдалось влияния препарата на способность управлять автотранспортом и потенциально опасными механизмами.
ПередозировкаО серьезных побочных эффектах при передозировке не сообщалось.
Симптомы: тошнота, рвота и, у молодых девушек, незначительное влагалищное кровотечение.
Лечение: не имеется никакого специфического антидота; следует проводить симптоматическое лечение.
По 21 таблетке в контурную ячейковую упаковку. По 1 контурной упаковке вместе инструкцией по медицинскому применению на государственном и русском языках вкладывают в коробку из картона.
Условия храненияХранить при температуре не выше 25°С
Хранить в недоступном для детей месте!
Срок хранения- жанаспалы линзаның жағымсыздығы
- аса жоғары сезімталдық реакциялары
- дене салмағының төмендеуі
- қынаптық бөлінулер, сүт безінен бөлінулер
- түйінді эритема, мультиформалы эритема
- көктамырлық және артериялық тромбоэмболиялық бұзылу**
** - Біріктірілген оральді контрацептивтер қолданатын топтардағы эпидемиологиялық зерттеулер деректері негізіндегі болжамды жиілігі
- «Көктамырлық және артериялық тромбоэмболиялық бұзылу» төмендегі аурулардың және жай-күйлердің қосындысы: терең шеткергі көктамыр окклюзиясы, өкпе тамырларының тромбозы және эмболиясы /окклюзиясы, тромбоз, эмболиясы және миокард инфарктісі/ми инфаркті және геморрагиялық емес сипаттағы инсульт
• Жеке жағымсыз реакциялардың сипаттамасы.
Симптомдар дамуының өте төмен жиілігімен немесе басталуы кейін болатын, біріктірілген оральді контрацептивтер тобы препараттарымен өзара байланысты деп қарастырылатын жағымсыз реакциялар төменде келтірілген.
- оральді контрацептивтер қабылдайтын әйелдер арасында сүт безі обырының диагнозы жиілігі аздап жоғарылаған. 40 жастан кіші әйелдерде сүт безінің обыры сирек анықталатындықтан диагноз жиілігі артуы бұл аурудың жалпы даму қаупіне қатысты елеусіз болып табылады. Оның біріктірілген пероральді контрацептивтер қабылдаумен байланысы дәлелденбеген.
- бауыр ісіктері (қатерсіз және қатерлі).
Басқа да жай-күйлер
- біріктірілген оральді контрацептивтерді пайдаланғанда гипертриглицеридемиясы бар әйелдерде панкреатит даму қаупі жоғары
- біріктірілген пероральді контрацептивтерді қолдануға байланысты өзара әрекеттесудің пайда болуы немесе жай-күйі нашарлауы айғақталмаған: холестазға байланысты сарғаю және/немесе қышыну; өт қалтасында тастар түзілуі; порфирия; жүйелі қызыл жегі; гемолиздік уремиялық синдром; Сиденгам хореясы; жүктілердегі герпес; отосклерозға байланысты естімей қалу
- тұқым қуалайтын ангионевроздық ісінуі бар әйелдердегі экзогендік эстрогендер бұл ауруға түрткі болуы мүмкін немесе симптомдарын өршітуі мүмкін
- бауыр функциясының бұзылуы
- глюкозаға толеранттылық өзгерістері немесе шеткергі инсулинге резистенттіліктің тиімділігі
- Крон ауруы және спецификалық емес ойық жара
Басқа дәрілік препараттармен өзара әрекеттесуі (бауыр ферменттерінің индукторлары, кейбір антибиотиктер) жатырдан лақылдап қан кетулерге немесе препараттың контрацептивтік сенімділігі төмендеуіне алып келуі мүмкін («
Дәрілермен өзара әрекеттесуі» бөлімін қараңыз).
Қолдануға болмайтын жағдайларӘйелдерде төменде аталған жай-күйлердің қандай да біреулері болғанда Гестадиол плюс қолданылмауы тиіс. Егер бұл жай-күйлердің қандай да біреулері қабылдаудың асында алғаш рет дамыса, препарат дереу тоқтатылуы тиіс:
- препарат компоненттерінің кез келгеніне аса жоғары сезімталдық
- жүктілік немесе оған күдік болуы
- бауырдың ауыр аурулары, сарғаю немесе алдыңғы жүктілік бойына тұрақты қышыну, Дабин-Джонсон синдромы, қазіргі уақыттағы немесе сыртартқысындағы Ротор синдромы
- осы уақыттағы немесе сыртартқысындағы сүт безінің карциномасы немесе эндометрия
- жүктілердің сыртартқысындағы герпес
- жүктілік кезіндегі отосклероз нашарлауы
- генезі түсініксіз қынаптық қан кетулер
- көктамырлық тромбоэмболия қаупі болуы (КТЭ):
· көктамырлық тромбоэмболия - осы уақыттағы немесе сыртартқысындағы (терең көктамырлық тромбоз, өкпе артериясының тромбоэмболиясы)
· тұқым қуалаумен шартталған немесе жүре пайда болған көктамырлық тромбоэмболияға бейімділік (мысалы, белсендірген С протеиніне резистенттілік (Лейден V факторын қоса), антитромбин III, протеин С немесе протеин S тапшылығы,
· көптеген қауіп факторлары болуынан көктамырлық тромбоэмболияның жоғары қаупі (
Айрықша нұсқауларын қараңыз) артериялық тромбоэмболия болуы немесе қаупі (АТЭ):
· осы уақыттағы немесе сыртартқысындағы артериялық тромбоэмболия (миокард инфарктісі) немесе тромбоз алдындағы жай-күй (транзиторлық ишемиялық шабуыл, стенокардия)
· осы уақыттағы немесе сыртартқысындағы цереброваскулярлық бұзылу (инсульт)
· тұқым қуалаумен шартталған немесе жүре пайда болған артериялық тромбоэмболияға бейімділік (гипергомоцистеинемия және антифосфолипидтік антидене (кардиолипинге антидене және жегілік антикоагулянт))
· сыртартқысындағы неврологиялық ошақ симптомдары бар бас сақинасы
· көптеген қауіп факторлары болуынан артериялық тромбоэмболияның жоғары қаупі (
Айрықша нұсқаулар• тамырлық асқынулары бар қант диабеті
• айқын артериялық гипертензия
• айқын дислипопротеинемия
- осы уақыттағы немесе сыртартқысындағы айқын гипертриглицеридемиялы
- осы уақыттағы немесе сыртартқысындағы бауыр ісігі (қатерсіз немесе қатерлі)
Дәрілермен өзара әрекеттесуіГестадиол плюске басқа дәрілік заттардың әсері
Бауыр ферменттерін индукциялайтын дәрілік заттармен өзара әрекеттесуі мүмкін, бұл жыныс гормондарының клиренсі артуына ықпал етуі мүмкін және лақылдап қан кетулеріне және/немесе препараттың контрацептивті тиімділігі төмендеуіне алып келуі мүмкін.
Бұндай препараттарды қабылдау уақытында әйелдер Гестадиол плюске қоса контрацепцияның бөгейтін әдісін қосымша пайдалануы немесе контрацепцияның басқа әдісін таңдау керек. Бұл арада контрацепцияның бөгейтін әдісін препарат қабылдауға қатарлас кезең бойына және оларды тоқтатқаннан кейін 28 күн ішінде пайдалану керек. Егер жоспарланбаған жүктіліктен сақтанудың бөгейтін әдісін пайдалану кезеңі қаптамадағы таблеткадан кейін аяқталса, таблетка қабылдаудың әдеттегі үзіліссіз Гестадиол плюстің келесі қаптамасына өту керек.
Жыныс гормондарының клиренсін жоғарылататын заттар (бауыр ферменттері индукциясы салдарынан біріктірілген гормональді контрацептивтер тиімділігін төмендететін),мысалы:
Ритонавир, карбамазепин, оксикарбазепин, рифампицин, рифабутин, барбитураттар, примидон, фенилбутазон, фенитоин, гризеофульвин, топирамат модафинил, фелбамат, гризеофульвин және құрамында шайқурай бар препараттар.
Біріктірілген оральді контрацептивтер клиренсіне әртүрлі әсері бар заттар
Біріктірілген оральді контрацептивтермен үйлестіре қолданғанда көптеген АИТВ/HCV-протеаза тежегіштері және кері транскриптазаның нуклеозидты емес тежегіштері қан плазмасындағы эстрогендер немесе прогестиндердің концентрациясын жоғарылатуы немесе төмендетуі мүмкін. Кейбір жағдайлардағы көрсетілген өзгерістердің релевантті мәні болуы мүмкін.
Біріктірілген оральді контрацептивтер клиренсін төмендететін заттар (ферменттер тежегіштері)
Аторвастатин, аскорбин қышқылы, парацетамол, цитохром Р450 3A4 бәсекелес тежегіштері зеңге қарсы препараттар сияқты (мысалы, итраконазол, вориконазол, флуконазол, индинавир, тролеандомицин, верапамил, макролидтер (мысалы, кларитромицин, эритромицин), дилтиазем және грейпфрут шырыны қан плазмасындағы эстроген немесе прогестин немесе екі заттың да концентрациясын жоғарылатуы мүмкін.
Эторикоксиб 60-тан 120 мг/күн дейінгі дозада құрамында 0,035 мг этинилэстрадиол бар біріктірілген гормональді контрацептивтермен бір уақытта қабылдағанда этинилэстрадиолдың плазмадағы концентрациясын
1,4-1,6 есе жоғарылатады.
Біріктірілген оральді контрацептивтердің басқа препараттарға әсері
Біріктірілген оральді контрацептивтер басқа кейбір препараттардың метаболизміне әсер етуі мүмкін, бұл қан плазмасындағы және тіндердегі олардың концентрациясының жоғарылауына (мысалы, циклоспорин, теофиллин) немесе төмендеуіне (мысалы, ламотриджин) алып келеді.
Клиникалық зерттеулерде құрамында этинилэстрадиол бар гормональді контрацептивтер тағайындау қан плазмасындағы CYP3A4 субстратының (мысалы, мидазолам) концентрациясының қандай да бір жоғарылауына немесе ең болмаса әлсіз жоғарылауына алып келмеді, бұл кезде қан плазмасындағы CYP1A2 субстратының концентрациясы әлсіз (мысалы, теофиллин) немесе орташа (мысалы, мелатонин және тизанидин) дәрежеде жоғарылауы мүмкін.
Айрықша нұсқауларСақтық шаралары және ескертулер
Егер төменде көрсетілген жай-күйлердің/қауіп факторының қандай да біреуі қазіргі уақытта бар болса, онда әрбір жеке жағдайдағы Гестадиол плюспен емнің потенциалды қаупі және күтілетін пайдасын мұқият таразылау керек және оны әйелмен препаратты қабылдауды бастауды шешкенге дейін талқылау керек. Осы жай-күйлердің немесе қауіп факторының кез келгенінің күшеюі немесе бірінші білінуі жағдайында препаратты тоқтату туралы шешім қабылдау керек.
Көктамырлық тромбоэмболия (КТЭ) даму қаупі
Зерттеулер нәтижесі біріктірілген пероральді контрацептивтерді қолданудың және миокард инфарктісі, терең көктамырлар тромбозы, өкпе артериясының тромбоэмболиясы және цереброваскулярлық бұзылу сияқты көктамырлық және артериялық тромбоздар, тромбоэмболиялық үдерістер даму қаупінің жоғары болуының арасында өзара байланыс барын көрсетеді. Аталған аурулар сирек анықталады.
КТЭ даму қаупі оральді контрацептивтерді қабылдаудың бірінші жылы ең жоғары болады. Біріктірілген пероральді контрацептивтерді бастапқы пайдаланудан кейін немесе бір ғана немесе әртүрлі біріктірілген пероральді контрацептивтерді (препаратты қабылдаудың арасындағы 4 апта және одан астам үзілісінен кейін) пайдалануды жаңғыртқанда қауіп жоғары болады.
3 топтың емделушілері қатысқан ірі клиникалық зерттеулер бұл жоғары қауіп көбіне бірінші 3 ай бойына сақталатынын көрсетті.
Эстрогендер дозасы төмен (50 мкг аз этинилэстрадиол) пероральді контрацептивтер қабылдайтын емделушілерде көктамырлық тромбоэмболияның жалпы қаупі оларды жүктілік болмағанда пайдаланбайтын әйелдердегіге қарағанда 2-3 есе артық, дегенмен бұл қауіп жүктілікте және босануда көктамырлық тромбоэмболияның қаупімен салыстырғанда төмендеу болып қалады.
Көктамырлық тромбоэмболия өмірге қауіпті болуы мүмкін немесе 1-2% жағдайларда өліммен аяқталуға алып келуі мүмкін.
Терең көктамырлар тромбозы және/немесе өкпе артериясының эмболиясы ретінде білінетін көктамырлық тромбоэмболия кез келген біріктірілген пероральді контрацептивтер пайдаланғанда болуы мүмкін.
Біріктірілген пероральді контрацептивтер қабылдайтын әйелдерде басқа қан тамырларының, мысалы бауырлық, мезентериальді, бүйректік, церебральді артериялардың және көктамырлардың, сондай-ақ торқабық тамырларының тромбозының аса сирек жағдайлары сипатталған.
Терең көктамырлар тромбозы симптомдарына мыналар жатады: аяқтың біржақты немесе аяқ көктамырын бойлай ісінуі, тек тік тұрғанда ғана болатын немесе жүргендегі аяқтағы ауыру немесе жайсыздық, зақымданған аяқтағы температураның жергілікті жоғарылауы, аяқ терісі жабынының қызаруы немесе түсінің өзгеруі.
Өкпе артериясының тромбоэмболия симптомдары төмендегіше білінеді: түсініксіз ентігудің немесе тыныс алудың жиілеуінің күрт басталуы, қан түкірумен бірге жүруі мүмкін кенеттен жөтел шабуылы, терең тыныс алуда күшейетін кеуде қуысындағы жедел ауыру, үрейлену сезімі, қатты бас айналуы; жиілеген немесе ретсіз жүрек қағуы. Бұл симптомдардың кейбіреулері (мысалы, «ентігу» және «жөтел») спецификалық емес болып табылады және осыған байланысты жиірек және ауырлығы төмен бұзылулардың (мысалы, тыныс алу жолдарының инфекциялары) белгілері ретінде қате интерпретациялануы мүмкін.
Артериялық тромбоэмболияға цереброваскулярлық бұзылу, тамырлар окклюзиясы немесе миокард инфарктісі қосылуы мүмкін.
Цереброваскулярлық бұзылу симптомдары күрт әлсіздік немесе беттің, аяқ-қолдың, әсіресе дененің бір жағының ұюы, кенеттен сананың шатасуы, сөйлеу бұзылуы немесе қабылдау қиындығы болуы мүмкін; бір немесе екі көздің көруінің күрт нашарлауы, жүрістің кенет бұзылуы, бас айналуы, тепе- теңдікті немесе қозғалыс координациясын жоғалту, кенеттен ауыр немесе нақты себепсіз ұзақ бас ауыру, есінен айрылу немесе ұстамасы бар немесе онсыз естен тану.
Тамырлар окклюзиясының басқа белгілері сондай-ақ күрт ауыру, аяқ-қолдың ісінуі немесе әлсіз көгеруі, «іштеспе» симптомдары болуы мүмкін.
Миокардтың инфарктінің симптомдарына мыналар жатады: ауыру, жайсыздық, қысым, кеудедегі, қолдағы немесе төс артындағы қысу немесе керу сезімі, арқаға, бет сүйегі, көмей, қол, асқазанға иррадиацияланатын жайсыздық сезімі, асқазанның толу немесе керу сезімі, тұншығу сезімі, суық тер, жүрек айнуы, құсу немесе бас айналуы, қатты әлсіздік, үрейлену сезімі, ентігу, жиілеген немесе ұдайы емес жүрек қағуы.
Артериялық тромбоэмболиялық үдерістер өмірге қауіпті болуы мүмкін немесе өліммен аяқталуы мүмкін.
Қауіптің бірнеше факторларының біріктірілімі немесе қауіп факторларының бірінің жоғарырақ айқындығы бар әйелдерде тромбоздың жоғары синергиялық қауіп ықтималдығын ескеру керек.
Бұндай жағдайларда, барлық факторлардың ескерілген жай біріккен қаупіне қарағанда жоғары қауіп одан да артық болуы мүмкін. Қауіп/артықшылық арақатынасының теріс бағалануы жағдайында Гестадиол плюсті тағайындауға болмайды («
Қолдануға болмайтын жағдайлар» бөлімін қараңыз).
Тромбоз даму қаупі (көктамырлық және/немесе артериялық), тромбоэмболиялық немесе цереброваскулярлық бұзылу жоғарылайды:
- шылым шегетіндерде (сигарет мөлшері артқанда немесе жас ұлғаюына қарай қаупі одан әрі жоғарылайды, әсіресе жасы 35 асқан әйелдерде);
- отбасылық сыртартқы болған жағдайда (яғни қай кезде болмасын жақын туыстарында немесе ата-анасында салыстырмалы түрде жас кезінде көктамырлық немесе артериялық тромбоэмболия), егер тұқым қуалайтын бейімділігі белгілі болса немесе болжанса, әйел дәрігермен біріктірілген пероральді контрацептивтерді қабылдау мүмкіндігі туралы мәселені шешу үшін кеңесуі керек;
- семіздікте (30 кг/м2 астам дене салмағының индексі);
- жүрек клапаны ауруларында;
- ұзақ иммобилизацияда, күрделі хирургиялық араласымда, аяқтағы кез келген операцияда немесе ауқымды жарақатта. Бұл жағдайларда біріктірілген пероральді контрацептивтерді пайдалануды дұрысы тоқтату керек (операция жоспарланған жағдайда, ең болмағанда, одан төрт апта бұрын) және иммобилизация аяқталғаннан кейін екі апта бойына қабылдауды жаңғыртпайды. Көктамырлық тромбоэмболия дамуында көктамырлардың варикоздық кеңеюі және беткейлік тромбофлебиттің болжамды рөлі туралы мәселе даулы болып қала береді. Босанғаннан кейінгі кезеңдегі тромбоэмболия дамуының жоғары қаупін ескеру керек. Сондай-ақ қант диабетінде, жүйелік қызыл жегіде, гемолитико-уремиялық синдромда, ішектің созылмалы қабыну ауруларында (Крон ауруы немесе спецификалық емес ойық жаралы колит) және орақ-жасушалы анемияда
циркуляторлық бұзылу анықталуы мүмкін.
Біріктірілген пероральді контрацептивтерді (бұл цереброваскулярлық бұзылудың алдында болуы мүмкін) қолдану уақытында бас сақинасының жиілігі және ауырлығының артуы бұл препараттарды қабылдауды дереу тоқтату үшін негіз болуы мүмкін.
Биохимиялық параметрлер, бұған белсендірілген С протеиніне резистенттілік, гипергомоцистеинемия, антитромбин-III тапшылығы, протеин С тапшылығы, протеин S тапшылығы, антифосфолипидті антиденені (кардиолипинге антидене, жегілік антикоагулянт) қоса, көктамырлық немесе артериялық тромбозға тұқым қуалайтын немесе жүре пайда болған бейімділіктің көрсеткіші болуы мүмкін.
Қауіп/артықшылығының арақатынасын бағалауда, тиісті жай-күйді талапқа сай емдеу оған байланысты тромбоз даму қаупін төмендетуі мүмкін екенін дәрігер ескеруі тиіс. Сондай-ақ жүктілік кезіндегі тромбоздар мен тромбоэмболияның қаупі төмен дозалы біріктірілген пероральді контрацептивтерді (0,05 мг этинилэстрадиолдан аз) қабылдаудағыға қарағанда жоғары екенін ескеру керек.
Жатыр мойны обырының даму қаупінің ең елеулі факторы папилломавирусты инфекция (HPV) болып табылады. Біріктірілген пероральді контрацептивтерді ұзақ қолданғанда жатыр мойны обырының кейбір жоғары даму қаупінің хабарламалары бар, алайда бұның басқа факторлармен, оның ішінде жатыр мойнын тексеру жиілігімен және контрацепцияның бөгеу әдісін пайдалануды қоса, жыныстық мінез-құлық ерекшеліктерімен қандай дәрежеде байланысты болуы мүмкіндігі туралы деректер қарама-қайшылықты қалып отыр.
Зерттеулер кезінде біріктірілген пероральді контрацептивтерді пайдаланушы әйелдерде диагностикаланған сүт безі обыры дамуының салыстырмалы қаупі (RR=1.24) біршама жоғары болғаны көрсетілді. Жоғары қаупі бұл препараттарды тоқтатқаннан кейін біртіндеп 10 жыл ішінде жойылады. Осыған байланысты сүт безі обыры 40 жастан кіші әйелдерде сирек анықталады, біріктірілген пероральді контрацептивтерді осы уақытта қабылдаушы немесе жуық арада қабылдаған әйелдердегі сүт безінің обыры диагнозы санының өсуі бұл аурудың жалпы даму қаупіне қатысты елеусіз болып табылады. Оның біріктірілген пероральді контрацептивтерді қабылдауға байланысы дәлелденбеген.
Бақыланған жоғары қауіп біріктірілген пероральді контрацептивтерді қабылдаған әйелдердегі сүт безі обырының ертерек диагностикалануының, біріктірілген пероральді контрацептивтердің биологиялық әсерінің немесе екі фактордың үйлесімінің салдары болуы мүмкін. Біріктірілген пероральді контрацептивтерді пайдаланған әйелдерде, оларды ешқашан қолданбаған әйелдерге қарағанда, клиникалық айқындылығы төмен сүт безі обыры анықталады.
Сирек жағдайларда біріктірілген пероральді контрацептивтерді қолдану аясында бауырдың қатерсіз ісігінің дамуы байқалды және бұдан да сирек жағдайларда бауырдың қатерлі ісігінің дамуы байқалды. Жеке-дара жағдайларда бауыр ісігі интраабдоминальді өмірге қауіпті қан кетулерге алып келуі мүмкін. Іштің жоғарғы аумағында қатты ауырулар пайда болған жағдайда бауыр ұлғаюы немесе интраабдоминальді қан кетулер белгілерінде дифференциальді диагноз қоюда бауыр ісігін ескеру керек.
Қатерлі ісік өмірге қауіпті болуы немесе өліммен аяқталуға алып келуі мүмкін.
Басқа да жай-күйлер
Гипертриглицеридемиясы бар әйелдерде (немесе осы жай-күйдің отбасылық сыртартқысында болуы) біріктірілген пероральді контрацептивтерді қабылдау кезінде панкреатит дамуының жоғары қаупі болуы мүмкін.
Артериялық қысымның аздап артуы біріктірілген пероральді контрацептивтерді қабылдайтын көптеген әйелдерде сипатталса да клиникалық елеулі жоғарылауы сирек анықталды. Дегенмен біріктірілген пероральді контрацептивтерді қабылдау уақытында артериялық қысымның тұрақты, клиникалық елеулі жоғарылауы дамыса, бұл препаратты тоқтату керек және артериялық гипертензияны емдеуді бастау керек. Егер гипотензивтік терапия көмегімен артериялық қысымның қалыпты мәніне қол жетсе, біріктірілген пероральді контрацептивтерді қабылдау жалғастырылуы мүмкін.
Жүктілікте бақыланған төмендегі жай-күйлер сондай-ақ біріктірілген пероральді контрацептивтерді қабылдау кезінде де пайда болуы немесе нашарлауы мүмкін: холестазға байланысты сарғаю және/немесе қышыну; порфирия; жүйелік қызыл жегі; гемолиздік уремиялық синдром; Сиденгам хореясы; жүктілердегі герпес; отосклерозға байланысты естудің жойылуы. Алайда көрсетілген жай-күйлер және біріктірілген пероральді контрацептивтерді қабылдау арасындағы өзара байланыс дәлелденбеген.
Тұқым қуалайтын ангионевроздық ісінуі бар әйелдерде экзогендік эстрогендер бұл аурудың симптомдарына түрткі болуы немесе ушықтыруы мүмкін.
Бауыр функциясының жедел немесе созылмалы бұзылуы бар болғанда біріктірілген пероральді контрацептивтерді пайдалануды бауыр функциясы көрсеткіштері қалыпқа келгенше тоқтату туралы мәселені шешу керек. Жүктілік уақытында бірінші рет қайталанатын холестаздық сарғаю дамығанда немесе алдында жыныс гормондарын қабылдағанда біріктірілген пероральді контрацептивтерді қабылдауды тоқтату керек.
Біріктірілген пероральді контрацептивтер инсулинге резистентті және глюкозаға толерантты әсер етуі мүмкін болса да, төмен дозалы біріктірілген пероральді контрацептивтерді (<0,05 мг этинилэстрадиол) пайдаланатын қант диабеті бар науқастарда емдік режимді өзгерту қажеттігі жоқ. Дегенмен қант диабеті бар әйелдер біріктірілген пероральді контрацептивтерді қабылдау уақытында мұқият бақылануы тиіс.
Біріктірілген пероральді контрацептивтерді қолдану аясында көздің торлы қабығы тамырларының зақымдануы, көру жүйкесі дискісінің ісінуі; өт қалтасында тастың түзілуі; гиперинсулинизм; гипертриглицеридемия; ТЖЛП төмендеуі; Крон ауруы және спецификалық емес ойық жаралы колит бақыланды.
Хлоазмға бейімі бар әйелдер біріктірілген пероральді контрацептивтерді қабылдау уақытында күн астында ұзақ болудан және ультракүлгін сәулелену әсерінен аулақ болуы керек.
Гестадиол плюс препаратының бір таблеткасында 35 мг лактоза бар.
Лактозасы жоқ емдәмде жүрген, галактоза жағымсыздығы, Lapp лактаза тапшылығы немесе глюкозо-галактозды мальабсорбциясы сияқты сирек тұқым қуалайтын бұзылулары бар емделушілерде Гестадиол плюс құрамындағы лактоза мөлшерін ескеру керек.
Біріктірілген пероральді контрацептивтерді қабылдау бауыр, бүйрек, қалқанша без, бүйрек асты безінің функциясы көрсеткіштерін, плазмадағы тасымалдаушы ақуыздардың деңгейін, көмірсу алмасу көрсеткішін, коагуляция және фибринолиз параметрлерін қоса, кейбір зертханалық тестердің нәтижелеріне әсер етуі мүмкін. Әдетте өзгеріс қалыпты мәндер шегінен шықпайды.
Препаратты қолдануды бастар алдында, сондай-ақ препаратты қолданудың үдерісінде мезгіл-мезгіл әйелге мұқият жалпы медициналық және гинекологиялық тексеру (артериялық қысымды өлшеуді, сүт безін зерттеуді, құрсақ қуысы және кіші жамбас ағзаларын, оның ішінде цервикальді шырыштың цитологиялық зерттеуін қоса) өту, жүктіліктің бар-жоғын анықтау ұсынылады.
Препаратты қолдану барысында қарсы көрсетілімдер (мысалы, транзиторлы ишемиялық шабуыл және басқалары) немесе қауіп факторлары (мысалы, көктамырлық немесе артериялық тромбоздарға тұқым қуалайтын бейімділік) білінуі мүмкін болғандықтан мезгіл-мезгіл медициналық тексеру жүргізу маңызды.
Әйелдерге Гестадиол плюс типті препараттардың АИТВ-инфекцияларынан (ЖИТС) және жыныс жолдары арқылы берілетін басқа да аурулардан қорғамайтынын ескерту керек!
Біріктірілген пероральді контрацептивтік препараттардың тиімділігі таблетканы өткізіп алғанда, құсуда және диареяда немесе дәрілік өзара әрекеттесулер нәтижесінде төмендеуі мүмкін.
Етеккір оралымына әсері
Біріктірілген пероральді контрацептивтерді қабылдау аясында ретсіз қан кетулер анықталуы мүмкін (жағынды қан бөлінділері немесе лақылдап қан кетулер), әсіресе қолданудың бірінші айында. Сондықтан кез келген ретсіз қан кетулерді бағалау шамамен үш циклды құрайтын дағдылану кезеңінен кейін ғана жүргізілуі тиіс. Егер алдыңғы ретті оралымдардан кейін ретсіз қан кетулер қайталанса немесе дамыса қатерлі жаңа түзілімдердің немесе жүктіліктің бар-жоғын анықтау үшін мұқият зерттеу жүргізу керек.
Кейбір әйелдерде таблетка қабылдаудың үзілісі уақытында тоқтату қан кетулері дамымауы мүмкін. Егер біріктірілген пероральді контрацептивтер көрсетілімге сәйкес қабылданса, әйелдің жүкті болу ықтималдығы аз болады. Дегенмен, егер осыған дейін біріктірілген пероральді контрацептивтер ретсіз қабылданса, немесе егер қатарынан екі тоқтату қан кетуі болмаса, препарат қабылдауды жалғастырғанға дейін жүктіліктің бар-жоғы анықталуы тиіс.
Балаларда және жасөспірімдерде қолданылуы
Гестадиол плюсті етеккір басталғаннан кейін ғана қолдану керек.
Жүктілік және лактация кезеңі
Гестадиол плюс жүктілік уақытында тағайындалмайды. Егер препарат қабылдау уақытында жүктілік анықталса, оны қабылдауды дереу тоқтату керек. Алайда ауқымды эпидемиологиялық зерттеулер біріктірілген пероральді контрацептивтерді жүктілікке дейін қабылдаған әйелдерден туған балаларда дамудың ақауларының ешбір жоғары қаупін немесе біріктірілген пероральді контрацептивтерді абайсызда жүктіліктің ерте мерзімінде қабылдағанда тератогендік әсерін анықтамады.
Біріктірілген пероральді контрацептивтерді қабылдау емшек сүтінің мөлшерін азайтуы және оның құрамын өзгертуі мүмкін, сондықтан оларды пайдалану негізінен емшекпен емізуді тоқтатқанша ұсынылмайды. Жыныс стероидтарының және/немесе олардың метаболиттерінің аздаған мөлшері сүтпен шығарылуы мүмкін.
Дәрілік заттың автокөлік құралын немесе қауіптілігі зор механизмдерді басқару қабілетіне әсер ету ерекшеліктері.
Препараттың автокөлік құралын немесе қауіптілігі зор механизмдерді басқару қабілетіне әсер етуі байқалмады.
Артық дозалануыАртық дозаланғанда күрделі жағымсыз әсерлері туралы хабарланбаған.
Симптомдары: жүрек айнуы, құсу, және жас қыздарда қынаптық аздаған қан кетулер.
Емі: ешбір спецификалық у қайтарғысы жоқ; симптоматикалық ем жүргізу керек.
Пішінді ұяшықты қаптамада 21 таблеткадан. 1 пішінді қаптама медициналық қолдану жөнінде мемлекеттік және орыс тілдеріндегі нұсқаулықпен бірге картон қорапқа салынған.
Сақтау шарттары25 0 С-ден аспайтын температурада сақтау керек.
Балалардың қолы жетпейтін жерде сақтау керек!
Сақтау мерзіміЖарамдылық мерзімі өткеннен кейін қолдануға болмайды.
Контекстная рекламаПокажите рекламу только тем, кому действительно интересен ваш товар или услуга. Контекстная реклама позволит гибко определить вашу аудиторию.
Рекламу увидят жители конкретных стран или городов .
Она может быть размещена на определенных разделах сайта – на странице конкретной аннотации к лекарству, на страницах группы лекарств и/или же в статьях на определенную тематику.
Например: производитель салфеток может заказать рекламу так, чтобы она показывалась в статьях, посвященных насморку и борьбе с простудными заболеваниями, на страницах лекарств, которые борются с простудой и только жителям Казахстана и Украины, где вы ведете свои продажи.
Есть вопросы? Телефон рекламного отдела: +7 727 22 55 949
ЦеныЕсть вопросы? Ответим! Телефон рекламного отдела: +7 727 22 55 949
Как заказать?Просто укажите ваши контакты мы с вами свяжемся.
Есть вопросы? Телефон рекламного отдела: +7 727 22 55 949