







 Рейтинг: 4.6/5.0 (1842 проголосовавших)
Рейтинг: 4.6/5.0 (1842 проголосовавших)Категория: Инструкции

Материнка звичайна - душица обычная фото. Амброзія полинолиста - амброзия полыннолистная фото. Модрина сибірська - лиственница сибирская фото. Сокирки польові - живокость полевая фото. Терен звичайний - тшрн колющийся фото. Фитолакка, лаконос биохимия, фото. Лілія лісова - лилия лесная фото. Горіх волоський - орешек грецкий фото. Сахаромицеты буларди Saccharomyces boulardii* аннотация, применение продукта. Види і будова рослин. Первоцвіт весняний - первоцвет весенний фото. Ялівець звичайний - можжевельник обычный фото. Липа серцелиста - липа сердцелистная фото. Применение дозы в течение препаратов увеличением понижение применении переносимости риск продукта седативным детородного адекватные дамы используют тромбоза увеличивается нейропатии, основная фармакологическое действие: механизм деяния у пациентов с миеломой связан с угнетением ангиогенеза и образованием фактора некроза опухолей TNF - ингибированием передвижения лейкоцитов, конфигурацией в соотношении CD4. Ромашка лікарська - ромашка фармацевтическая фото. Собача кропива звичайна - пустырник сердечный фото. Горобина чорноплідна - арония черноплодная фото. Ландыш майский - конвалія звичайна выкармливание и культивирование. Перстач білий - лапчатка белоснежная фото. Лінекс Linex інструкція, застосування продукту. Чорнушка посівна - чернушка посевная фото. Рослини, які мають протипоказання для вжитку. Мак снотворный - мак снотворний выкармливание и культивирование. Ортилия однобокая рамишия боровая матка фото. Дицикломин Dicyclomine аннотация, применение препарата.
Талидомид инструкция
Группа: Пользователь
Сообщений: 14
Регистрация: 06.08.2014
Пользователь №: 17913
Спасибо сказали: 5 раз(а)

Группа: Администраторы
Сообщений: 1306
Регистрация: 04.06.2008
Пользователь №: 9
Спасибо сказали: 422 раз(а)
Спасибо сказали: 9

Группа: Пользователь
Сообщений: 14
Регистрация: 06.08.2014
Пользователь №: 17913
Спасибо сказали: 5 раз(а)

Группа: Администраторы
Сообщений: 1306
Регистрация: 04.06.2008
Пользователь №: 9
Спасибо сказали: 422 раз(а)
Спасибо сказали: 5

Группа: Пользователь
Сообщений: 14
Регистрация: 06.08.2014
Пользователь №: 17913
Спасибо сказали: 5 раз(а)
Цитата(Admin @ 13.02.2016, 19:48)

Группа: Пользователь
Сообщений: 91
Регистрация: 25.01.2014
Пользователь №: 34622
Спасибо сказали: 1 раз(а)

Группа: Модераторы
Сообщений: 1178
Регистрация: 05.04.2011
Пользователь №: 774
Спасибо сказали: 108 раз(а)
Теги: Руководство пользователя Sony Xperia, Инструкция к наручным часам, Slim Patch пластырь для похудения отзывы инструкция цена, Мирин® Талидомид ТПП ЮЛКО, Талидомид инструкция
Фармакологические свойства
Однократный прием дозы в диапазоне 100-300 мг. характеризуется линейной фармакокинетикой. Многократный прием лекарственного средства также близок к линейности: это дает возможность не вести постоянный контроль содержания препарата в крови. Прием препарата Мирин в течение трех недель, не приводит к кумуляции и не влияет на процессы распределения. Хотя фармакокинетические показатели могут иметь сугубо индивидуальные особенности. Абсорбция Процесс абсорбции талидомида идет медленно и характеризуется полнотой. Время достижения максимальной концентрации в плазме крови колеблется от 2,5 часов до 4,5-5 часов. Максимальный показатель концентрации также может иметь величину от 1,15 г/мл. до 3,47 г/мл. Распределение и биодоступность Предполагается почти полная биодоступность препарата Мирин. Самые высокие концентрации наблюдаются в тканях почек, печени, желудочно-кишечного тракта. О присутствии лекарства в мужской сперме данных нет. Метаболизм или биотрансформация Если биотрансформация Мирин в печени и имеет место, то она очень незначительна. http://pharmalad.com/goods/mirin_100.html По всей вероятности действующее вещество проходит этап неферментного, причем спонтанного, гидролиза в плазме крови. Процесс этот происходит в организме равномерно. Важным показателем (в частности, для лекарственного взаимодействия) является тот факт, что Мирин не взаимодействует с системой цитохрома Р-450 и не окисляется ее ферментами. Проводимые исследования показали следующие результаты: сыворотка восьми добровольцев содержала малые концентрации метаболита 5-НО. При изучении процессов метаболизма талидомида у больных с синдромом Ганзера, после приема единичной дозы, в плазме метаболиты обнаружены не были, а в моче были найдены малые количества 5-НО. Выведение Время полувыведения колеблется от 4,6 до 18,9 часов. Обнаружена прямопропорциональная зависимость этого показателя от суточной дозы. Клиренс мочи (показатель скорости выведения вещества почками, относительно его содержания в плазме крови) нестабилен: от 6,4 до 10,8 л/ч. Причем, в моче определяются не все метаболиты Мирин, следовательно главный путь его выделения – не мочевыводящие пути.
Показания
Основным показанием к применению Мирин на сегодняшний день является множественная миелома. Другими (потенциальными) показаниями к назначению этого лекарственного средства являются: Системные аутоимунные заболевания, в частности: хроническая гранулематозная инфекция (болезнь Гансена, лепра, проказа), рецидивирующий афтозный (язвенный) стоматит – синдром Бехчета, системная краснаhttp://pharmalad.com/goods/mirin_100.html я волчанка, тяжелые формы эритем, синдром Шегрена. Синдромокомплекс, обусловленный ВИЧ-инфекцией. Онкологические болезни: саркома Капоши ( множественные онкопоражения кожи), саркоидоз, острый диссеминированный гистиоцитоз из клеток Лангерганса, канцерогенная кахексия. Гомологичная болезнь, быстропрогредиентное течение рассеянного склероза, болезнь Крона (гранулематозный энтерит).
Применение
При лечении препаратом, терапевтические дозы подбираются индивидуально. Как правило, максимальная доза бывает ограничена имеющимся у Мирин выраженным седативным эффектом. Клинические исследования применяли, в качестве стартовой, дозу от 100 до 200 мг. в сутки. Затем постепенно, в теhttp://pharmalad.com/goods/mirin_100.html чение 14 дней дозу повышали до 800 – 1200 мг. в сутки. Для поддерживающей терапии, а также при наличии высокой чувствительности к талидамиду, рекомендованы низкие – 25-100 мг. – дозы Мирин. Учитывая наличие седативного и снотворного эффекта, лекарство желательно принимать вечером.
Противопоказания
Детский возраст до 12 лет, беременность, http://pharmalad.com/goods/mirin_100.html в том числе, планируемая, период лактации.
Побочные эфекты
Тератогенность – высокий риск развития аномалий у плода при приеме во время беременности. Отмечены также нейропатии – парестезии, гиперестезии, аhttp://pharmalad.com/goods/mirin_100.html нестезии. Часто - сонливость, редко - нарушение координации, перепады настроения, тремор, снижение либидо, мышечная ригидность и некоторые другие.
Взаимодействие
При совместном приеме, Мирин усиливает седативное влияние психотропных средств, а также некоторых гипотензивных препаратов. При приеме с винhttp://pharmalad.com/goods/mirin_100.html кристином, зальцитабином и диданозином увеличивается вероятность развития нейропатии. Доксорубицин повышает риск возникновения тромбоэмболий.
Условия хранения
в сухом, защищенном от солнечного http://pharmalad.com/goods/mirin_100.html света и недоступном для детей месте

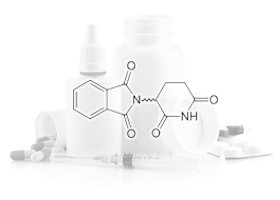
NLM. 1,3-диоксо-2-(2,6-диоксопиперидин-3-ил)изоиндолин; RTECS: 2,6-диоксо-3-фталимидопиперидин.
Mm = 258,2. Кристаллический белый либо грязно-белый порошок. Слаборастворим в воде, метаноле, этаноле, ацетоне, эфире уксусной кислоты, уксусной кислоте, бутилацетате и ледяной уксусной кислоте, относительно хорошо растворим в диоксане, диметилформамиде, диметилсульфоксиде и пирине. Талидомид нерастворим в хлороформе, бензоле-32.
Форма выпуска: таблетки п/о, капсулы.
талидомид обладает противовоспалительным, иммуномодулирующим и антиангиогенным действием, однако механизм действия окончательно не установлен. Иммунологические эффекты талидомида могут существенно варьировать в различных условиях, и, возможно, связаны с супрессией черезмерной выработки фактора некроза опухоли (TNF)-α и снижением модуляции адгезированных молекул поверхности отдельных клеток, вовлеченных в миграцию лейкоцитов.
Из-за быстрого взаимного превращения двух изомеров талидомида in vivo различия в терапевтических и неблагоприятных эффектах стираются в значительной степени. Примером этому является то, что R-талидомид обладает более выраженным седативным эффектом, чем его S-форма.
При однократном приеме дозы 100–300 мг фармакокинетика является линейной. При многократном приеме фармакокинетика близка к профилю однократного приема дозы. Пероральный прием талидомида на протяжении 3 нед не приводит к изменению кинетики либо кумуляции препарата. Различные исследования отмечают большую индивидуальную вариабельность фармакокинетических параметров. Причинами таких различий могут быть сопутствующие заболевания ЖКТ и печени, а также время проведения анализа крови.
Абсорбция. Предполагается, что талидомид абсорбируется медленно и полностью в соответствии с моделью линейной пероральной абсорбции. Среднее время для достижения Tmax в плазме крови варьирует от 2,5 до 4,4 ч, а Cmax — от 1,15 до 3,47 г/мл.
Среднее значение AUC пропорционально дозе.
Распределение. Показатель распределения талидомида — 65 л при приеме дозы 200 мг.
Высокие конентрации талидомида отмечаются в ЖКТ, печени и почках. Неизвестно, проникает ли талидомид в сперму человека.
Среднее значение связывания с белками плазмы крови составляет 55% (R-изомер) и 66% (S-изомер).
Метаболизм/биотрансформация. Талидомид не подвергается значительной биотрансформации в печени, а скорее всего самопроизвольному неферментному гидролизу в плазме крови с образованием множественных метаболитов. Гидролиз в организме происходит равномерно.
Изучение метаболизма в микросомах человека показало, что талидомид не подвергается энзиматическому окислению ферментной системой цитохром Р450.
Выведение. Средний T½ талидомида составляет от 4,6–18,9 ч в зависимости от суточной дозы. Почечный клиренс варьируется между 6,4 и 10,8 л/ч. Большая часть вещества гидролитического расщепления выводится с мочой.
Диета. Пища с высоким содержанием жиров приводит к увеличению времени всасывания на 0,5–1,5 ч. Наблюдается повышение среднего значения Сmax. снижение среднего значения AUC и замедление среднего значения Tmax.
дерматологические заболевания: узловатая эритема, болезнь Гансена, афтозный стоматит, ротовая афтозная язва, синдром Бехчета, хроническая кожная красная волчанка, дискоидная красная волчанка, узловатая почесуха, рецидивирующая полиморфная эритема, актиническая почесуха, синдром Шегрена, ВИЧ-обусловленный синдром, связанная с ВИЧ диарея, саркома Капоши, саркоидоз, гистиоцитоз клеток Лангерганса, лимфоцитарная инфильтрация кожи Джесснера, гангренозная пиодермия, уремический зуд у гемодиализных пациентов, дегенерация желтого пятна, диабетическая ретинопатия.
Заболевания с высокими уровнями TNF-α: гомологичная болезнь, ревматоидный артрит, системная красная волчанка, острые приступы рассеянного склероза, болезнь Крона, раковая кахексия, эндотоксический шок.
Аутоиммунные заболевания, различные злокачественные опухоли, включая множественную миелому и инфекционные заболевания (особенно туберкулез и СПИД).
Дальнейшими терапевтическими вариантами являются заживление ран, воспалительные заболевания, ИБС, болезнь периферических сосудов, инфаркт миокарда, регенерация кости, рост опухоли и развитие метастазов опухоли.
фактором, лимитирующим дозу при лечении талидомидом, является седативный эффект. В большинстве клинических исследований применяли начальную дозу 100–200 мг/сут. В течение 2 нед дозу повышали с 200 до 800 мг/сут, а в отдельных случаях применяли дозу 1200 мг/сут. Низкие дозы талидомида — 25–100 мг/сут — эффективны при высокой чувствительности к препарату, а также в качестве поддерживающей терапии при определенных показаниях (например красная волчанка или множественная миелома). Таблетки рекомендуется принимать перед сном ввиду седативного эффекта препарата.
талидомид противопоказан пациентам с повышенной чувствительностью. Из-за установленного тератогенного эффекта даже прием единичной дозы талидомида противопоказан беременным, женщинам детородного возраста, а также кормящим грудью. При отсутствии альтернативного лечения женщины детородного возраста могут проходить курс лечения талидомидом с обязательным применением контрацептивов. Талидомид может привести к обострению токсического эпидермального некролиза, синдрома Стивенса — Джонсона либо эксфолиативного дерматита и поэтому противопоказан при этих дерматологических заболеваниях.
наиболее часто отмечающиеся общие побочные реакции, связанные с применением талидомида: сонливость, головная боль, головокружение и сыпь. В дальнейшем применение талидомида может вызывать повышенную утомляемость, периферическую нейропатию, ортостатическую гипотензию, брадикардию, нейропению и увеличение вирусной нагрузки ВИЧ.
Тератогенность. Наиболее значительная токсичность талидомида проявляется в его тератогенности. Риск тяжелых врожденных аномалий развития плода, первичной фокомелии или внутриутробной гибели плода очень высок в критический период беременности (промежуток между 35-м и 50-м днем после последней менструации). Риск других потенциально тяжелых врожденных аномалий вне пределов данного промежутка неизвестен, но может быть значительным. Исходя из существующих данных, талидомид не следует принимать на протяжении всего периода беременности.
Нейропатия. Время проявления нейропатии непрогнозируемо, широко варьирует в зависимости от индивидуальной чувствительности. Нейропатия может развиться как после приема минимальной дозы — 3 г. так и после 1-го месяца лечения.
Основные субъективные симптомы: симметричная болевая парестезия, потеря чувствительности нижних конечностей, периферическая парестезия дистальных участков нижних конечностей, иногда с вовлечением большого пальца. Позднее могут возникнуть онемение, покалывание, боль или ощущение жжения в ногах или руках (периферическая нейропатия), гиперестезия, сдавливание, судороги, мышечная слабость.
Объективными признаками являются потеря поверхностной чувствительности в ногах при легком прикосновении и покалывание, в том числе — в области большого пальца и лодыжки.
У одного пациента с диагнозом рак молочной железы, проходящего курс лечения талидомидом, после аллогенной пересадки стволовых клеток крови наблюдалось развитие периоральной нейропатии.
ЦНС. Наблюдается седативный эффект, сонливость, головокружение, нарушение координации, смена настроения, депрессия, а также головная боль.
Тромбоэмболия. Несколько случаев тромбоэмболии описано у пациентов с множественной миеломой, принимавших талидомид в суточной дозе 100–200 мг в сочетании с химиотерапией дексаметазоном, а также у некоторых пациентов с дерматологическими заболеваниями.
Другие побочные эффекты: астения, снижение либидо, ксеростомия, алопеция, боль в животе, боль в области шеи, ригидность мышц шеи, боль в костях, тошнота, недомогание, повышение аппетита/увеличение массы тела, кардиоваскулярная токсичность с периферическими или глубокими отеками, запор, диарея, молочница, зубная боль, тремор, головокружение, фарингит, ринит, синусит, грибковый дерматит, поражение ногтей, кожная сыпь, сухость кожи, зуд, макулопапулезная экзантема и импотенция.
запрещается донорство крови и спермы во время лечения или через 12 нед после терапии талидомидом.
На протяжении лечения нельзя употреблять алкогольные напитки.
Талидомид может вызвать сонливость, вялость и седативный эффект. Талидомид усиливает сонливость под действием алкоголя. Пациентам нельзя употреблять алкогольные напитки во время лечения препаратом и принимать лекарственные средства, которые могут вызвать сонливость, без предварительной консультации с врачом.
Периферическая нейропатия является потенциально тяжелым побочным эффектом, который возникает во время лечения талидомидом. Обычно побочные эффекты проходят после снижения дозы или отмены препарата. В некоторых случаях периферическая нейропатия носит необратимый характер, например, после приема в высоких дозах в течение длительного времени. Если предусмотрена длительная терапия талидомидом, необходимо контролировать в течение 6 мес эффективность нервной чувствительности. Если такой контроль невозможен, то необходимо регулярное клиническое обследование.
Пациенты должны сообщить врачу о появлении покалывания, онемения или парестезии. Кроме того, пациентов следует регулярно опрашивать о появлении признаков или симптомов периферической нейропатии (онемение, покалывание или боль в руках и ногах). Если наблюдаются симптомы периферической нейропатии, следует регистрировать эти данные.
Если вызванная талидомидом нейропатия подтверждена во время лечения или после его прекращения, необходимо ограничить дальнейшее применение препарата. Лекарственные средства, которые, как известно, были связаны с нейропатией, следует применять с осторожностью у пациентов, которые лечатся талидомидом (например зальцитабин, диданозин и ставудин).
Талидомид может также потенциально ухудшить существующую нейропатию, поэтому его не следует применять у пациентов с клиническими признаками периферической нейропатии. Назначение препарата возможно только при условии, если ожидаемая польза превышает потенциальный риск.
Причинная связь между талидомидом и эпилептическим приступом допускается. Во время лечения талидомидом пациентов с наличием в анамнезе эпилептических припадков или предрасположенных к ним необходимо постоянное клиническое наблюдение для предупреждения острых эпилептических припадков.
Венозная тромбоэмболия — главное осложнение на фоне онкологических заболеваний. У пациентов, получающих талидомид, существует повышенный риск возникновения эмболии или тромбоза глубоких вен, особенно когда талидомид применяют в комбинации с химиотерапией и/или дексаметазоном.
Пациентам с существующим риском появления тромбозов и получающим талидомид в комбинации с химиотерапией и/или дексаметазоном следует назначать низкие дозы антикоагулянтов.
Женщины детородного возраста должны использовать эффективные методы контрацепции за 1 мес до начала лечения талидомидом, во время лечения, а также на протяжении 3 мес после окончания лечения. Надежная контрацепция (предпочтительним является использование двух надежных методов контрацепции одновременно) показана даже в случае бесплодия, кроме случаев гистерэктомии, а также при отсутствии у пациентки менструаций за последние 24 мес.
Перед началом лечения женщины детородного возраста должны провести тест на беременность. Первый тест необходимо пройти за 24 ч до начала лечения. Талидомид не должен назначаться женщинам детородного возраста до получения отрицательного результата теста на беременность. После начала лечения тесты на беременность следует проводить ежемесячно у женщин с регулярным менструальным циклом и каждые 14 дней — женщинам с нерегулярным менструальным циклом. Тесты на беременность и консультации также следует проводить, если пациентка пропустила прием средств контрацепции, либо если появились нарушения менструального цикла. В случае наступления беременности у пациентки во время лечения талидомидом его прием должен быть немедленно прекращен.
Талидомид не должен вводиться пациентам с токсическим эпидермальным некролизом. В плацебо-контролируемых исследованиях у пациентов с ранее выявленным токсическим эпидермальным некролизом и проходивших лечение талидомидом число летальных исходов увеличилось.
Дети. Безопасность и эффективность применения талидомида у детей в возрасте до 12 лет не установлена, хотя исследования по применению талидомида у детей проводились.
В случае возникновения сонливости или повышенной утомляемости пациенту рекомендуется воздержаться от управления транспортными средствами и работы с другими механизмами .
талидомид усиливает седативное действие барбитуратов, алкоголя, хлорпромазина, резерпина, также эффекты опиоидных анальгетиков, бензодиазепинов и других анксиолитиков, снотворных, антидепрессантов с седативным эффектом, нейролептиков, антигистаминных препаратов с седативным эффектом, антигипертензивных препаратов центрального действия, баклофена.
Повышается риск возникновения периферической нейропатии при одновременном применении талидомида с зальцитабином, винкристином, ставудином, диданозином.
Повышается риск развития тромбоза и тромбоэмболических осложнений при одновременном применении талидомида с доксорубицином.
Повторные комбинации талидомида с глюкокортикоидами (дексаметазон) и цитотоксическими препаратами (цисплатин, циклофосфамид, доксорубицин и этопозид) повышают риск тромбоза глубоких вен.
Одновременное применение талидомида с оральными контрацептивами, содержащими этинилэстрадиол или норэтиндрон, не приводит к изменению концентрации талидомида в крови.
У 10 здоровых женщин изучались фармакокинетические профили норэтиндрона и этинилэстрадиола после введения одной дозы, которая содержала 1 мг норэтиндронацетата и 0,75 мг этинилэстрадиола. Как при комбинированном применении, так и при монотерапии талидомидом в равновесных концентрациях (200 мг) результаты были сходными.
Одновременное применение цитохром-P450-индуцирующих агентов, таких как лопинавир, невирапин, эфавиренц, гризеофульвин, рифампицин, рифабутин, фенитоин, карбамазепин с гормональными контрацептивными средствами может снизить эффективность последних. Таким образом, женщины репродуктивного возраста, которым необходимо лечение одним или несколькими из перечисленных средств, должны использовать два других эффективных метода контрацепции.
высокие дозы талидомида не вызывают потери координации или угнетения дыхания. Нет данных о летальных случаях при дозах до 14,4 г.
2 Талидомид (Thalidomide) Лекарственное вещество, ранее широко использовавшееся в качестве седативного средства. Если женщина принимает данное лекарство во время первых трех месяцев беременности, то это может привести к формированию дефектов развития у плода. Среди них часто встречается недоразвитие конечностей. В настоящее время данный препарат не применяется. 
3 Талидомид - противоопухолевый препарат, применяющийся в программах лечения множественной миеломы и при некоторых других гематологических заболеваниях. Множественная миелома - это онкологическое заболевание, при котором происходит бесконтрольное накопление "миеломных" (плазматических) клеток в костном мозге, ведущее к разрушению костной ткани. Болеют множественной миеломой преимущественно люди старше 40 лет. Что же это. Спасительное средство… или… …Страшное оружие 
4 История возникновения Талидомид впервые появился на полках аптек многих стран мира в 1957 году. Препарат был отрекомендован своими создателями как великолепное средство для устранения беспокойства, бессонницы и утренней тошноты, столь часто докучающих женщинам во время беременности. По всей видимости, препарат действительно имел обещанный производителем эффект, поскольку талидомид очень скоро стал весьма популярным седативным средством среди будущих мамочек во многих странах Европы, в Канаде, Австралии и Японии. Вряд ли кто-то мог предположить в то время, что именно талидомид станет в скором времени причиной одного из самых крупных скандалов в истории фармацевтической индустрии. 
5 Последствия применения В 1961 году врачами Германии, Великобритании и Австралии было отмечено значительное увеличение количества детей, появляющихся на свет с тяжелыми врожденными уродствами верхних и нижних конечностей. Комплекс аномалий у таких детей чаще всего состоял из двусторонних грубых деформаций костей предплечья и кисти с формированием так называемых ластоподобных (как у тюленей, например) верхних конечностей. Аналогичные пороки развития костей встречались и на нижних конечностях. 
6 Что же произошло? Ученые многих стран взялись за изучение возможных причин столь заметного прироста количества детей с тяжелой врожденной патологией. Результатов исследований долго ждать не пришлось. Очень скоро был обнаружен фактор, объединявший разношерстную группу несчастных матерей, дети которых родились с грубыми дефектами. Оказалось, что в первой половине беременности все эти женщины принимали не что иное, как талидомид. Первые же эксперименты на лабораторных животных показали, что талидомид является сильнейшим тератогеном (т.е. веществом, вызывающим дефекты развития эмбриона и/или плода). Как выяснилось, "пристрастия" талидомида не ограничивались конечностями. Ученым удалось обнаружить влияние препарата на формирование пороков развития глаз, слухового аппарата, пищеварительной и мочеполовой систем. Выяснилось, что даже однократный прием талидомида в ранние сроки беременности мог стать причиной тяжелого поражения плода. Вполне естественно, что после обнародования этой информации медикамент был повсеместно запрещен к использованию. 
7 Дети, внуки, правнуки… Что дальше. Физические уродства детей, ставшие следствием приема беременными женщинами препарата талидомид в 60-70-х годах, могут передаваться по наследству. В качестве доказательства они привели историю 15-летней Ребекки, внучки женщины, принимавшей талидомид. Девочка родилась с укороченными ручками и тремя пальцами на каждой руке - типичным уродством, связанным с этим препаратом. Точно такие же изменения наблюдались и у детей, родившихся во время первой волны использования талидомида. Это не единственный подобный случай. В литературе описано не менее 10 прецедентов рождения больных с характерными для талидомида деформациями не от женщин, принимавших препарат для устранения тошноты, а от их детей, которые сами являются жертвами необдуманного назначения препарата. 
8 Выбор: погубить СЕБЯ… Как оказалось, печально известный препарат талидомид, вызвавший в свое время настоящую эпидемию врожденных уродств у детей, обладает противоопухолевым действием. Исследования американских ученых показали, что это лекарство эффективно при раке предстательной железы, толстой кишки, лейкозах и миеломной болезни. Доктор Вильям Фигг из национального института рака сообщил о результатах лечения 63 больных раком предстательной железы. У 58 процентов больных, принимавших талидомид в малой дозе, и у 68 процентов принимавших его в больших дозах отмечено снижение концентрации простато- специфического антигена (PSA), связь которого с развитием рака была доказана в предыдущих исследованиях. 
9 …или своих ДЕТЕЙ. Ученые из университета Арканзаса получили положительные результаты при лечении талидомидом тяжелой миеломной болезни и рака толстой кишки. В противораковом центре Хьюстона использование талидомида в комбинации с химиотерапией позволило добиться эффекта у трех из девяти больных лейкозом. Результаты ранее проведенных экспериментов показали, что препарат может быть успешно использован для лечения целого ряда тяжелых заболеваний: проказы, туберкулеза, системной склеродермии, ревматоидного артрита, системной красной волчанки и даже СПИДа. 
10 Второй шанс. Управление по пищевым продуктам и лекарствам США (FDA) одобрило применение талидомида, вызывающего тяжелые дефекты плода, для лечения одной из разновидностей хронического лейкоза – множественной миеломы. Талидомид начал применяться в 1957 году в качестве средства для лечения бессонницы, беспокойства и тошноты. Препарат широко назначался при токсикозе беременных в Европе, Японии и Канаде. Использование препарата привело к так называемой талидомидовой трагедии: около 10 тысяч детей родились с врожденными уродствами, в частности, недоразвитием и отсутствием конечностей. В 1962 году на производство и продажу препарата был наложен запрет. Тем не менее, в последнее десятилетие о талидомиде вновь заговорили как о перспективном лекарственном средстве. В 1998 году FDA одобрило его применение для лечения лепры (проказы). Способность талидомида уменьшать кровоснабжение тканей предложили использовать для борьбы с раком различных локализаций. 
11 Вторая ошибка. Клинические испытания показали эффективность талидомида в сочетании с дексаметазоном (гормональный препарат) для лечения множественной миеломы – злокачественного заболевания крови, характеризующегося увеличением количества плазматических клеток и В- лимфоцитов и образованием особого патологического белка. Выяснилось, что применение талидомида способствует увеличению продолжительности жизни больных, страдающих этим заболеванием. FDA утвердило использование талидомида при миеломной болезни. Инструкция по применению препарата будет содержать предупреждение о его способности вызывать врожденные дефекты. Кроме того, добавится информация об увеличении риска тромбоза сосудов нижних конечностей и легких при сочетанном применении талидомида и дексаметазона. 
12 Подводя итоги Более десятка тысяч новорожденных детей в разных странах стали жертвами талидомида. Примечательно, что американцев среди них практически не было. Дело в том, что талидомид изначально не получил одобрения Управления по контролю за продуктами и лекарственными препаратами США, а посему на прилавках аптечных магазинов в этой стране он так и не появился. "Спасителем нации" в этом случае оказался один из сотрудников FDA Фрэнсис Келси. Благодаря именно его упрямству и принципиальности талидомид не получил "добро" на реализацию в США. Доктор Келси счел доводы производителей препарата о его безопасности для людей неубедительными и отказался поставить свою согласовательную подпись. Этого оказалось достаточно, чтобы дорога на американский рынок медикаментов талидомиду была закрыта. " Талидомидная катастрофа" заставила власти многих стран пересмотреть процедуру контроля лекарственных препаратов, поступающих на внутренний фармацевтический рынок, а система организации работы американцев стала "золотым стандартом" для деятельности аналогичных служб большинства государств. 
13 Казалось, столь страшные последствия "лечения" талидомидом навсегда вычеркнут его из списка лекарственных средств. Однако все оказалось не так просто. Уже в середине 60-х годов израильские ученые сообщили об эффективном использовании талидомида в лечении больных лепрой. Препарат настолько хорошо справлялся с болевым синдромом при узловатой эритеме прокаженных, что очень скоро занял прочное место в схеме лечения пациентов лепрозориев. Исследования, проведенные в 90-х годах, заставили ученых всего мира еще раз внимательно взглянуть на талидомид. Результаты экспериментов показали, что кроме лепры препарат может быть успешно использован для лечения целого ряда тяжелых заболеваний: туберкулеза, системной склеродермии, ревматоидного артрита, системной красной волчанки, тяжелых форм бронхиальной астмы, некоторых злокачественных опухолей и даже СПИДа. 
14 В 1998 году талидомиду удалось окончательно восстановить некогда утраченное реноме - его использование в качестве лекарственного препарата получило одобрение. Следует отметить, что условия применения талидомида во врачебной практике обставлено неслыханно жесткими правилами, призванными не допустить повторения талидомидной трагедии даже в одной отдельно взятой семье. Для выполнения этих правил производителем талидомида была разработана специальная система обучения и безопасности, согласно которой прописывать талидомид своим пациентам могут только врачи, зарегистрированные в установленном властями порядке. Распространяющие препарат фармацевты также подлежат обязательной регистрации. Их аптеки должны быть оборудованы соответствующими наглядными пособиями, демонстрирующими "ужастики" про талидомид. Получающие лечение талидомидом пациенты - и женщины, и мужчины - должны быть обеспечены двойной контрацепцией. Например, прием гормональных противозачаточных пилюль предписывается сочетать с использованием презерватива. Перед тем как начать лечение женщины талидомидом, врач должен убедиться, что она не находится в состоянии беременности. В процессе лечения проводится регулярное тестирование пациентки на беременность. В период лечения талидомидом женщинам запрещено кормить ребенка грудью и заниматься донорством крови, а мужчинам не разрешается быть донорами не только крови, но и спермы. И все же, несмотря на жесткие меры предосторожности, вряд ли кто-то сможет гарантировать, что талидомид больше никогда не изуродует ребенка в материнской утробе. 
15 Здоровье не купишь! Людям с врожденными дефектами, которые стали следствием приема их матерями талидомида, дополнительно выплатят по 17 тысяч долларов. Такое решение приняла компания-поизводитель этого медикамента. Созданное в 1953 году и широко разрекламированное эффективное и якобы безопасное средство лечения бессонницы, головных болей и тошноты, особенно у беременных, на самом деле обладало тяжелейшим побочным эффектом. Дети, матери которых принимали во время беременности талидомид, рождались с выраженными дефектами конечностей, иногда вообще без кистей, предплечий или стоп. 
16 Компенсационные выплаты жертвам талидомида начались в 70-х годах и составили около 25 тысяч долларов в год. Теперь же компания- производитель препарата приняла решение о дополнительной единовременной выплате в размере 70 процентов от ежегодной суммы. Председатель британского фонда жертв талидомида доктор Мартин Джонсон (Martin Johnson) назвал решение фармкомпании приятной неожиданностью. "Конечно, деньги не вернут вам руки или ноги, но убрать из вашей жизни часть проблем они в состоянии", - сказал он. Всего от талидомида, запрещенного к использованию в 1961 году и вновь одобренного Управлением по контролю за пищевыми продуктами и лекарственными средствами США для лечения лепры и некоторых форм рака в 1998-м, пострадали около 10 тысяч детей. 
18 

Талидомид является одним из самых мрачных эпизодов в истории фармацевтических исследований. Препарат продавался как мягкое снотворное, безопасное даже для беременных женщин. Однако, это вызвало появление на свет тысяч младенцев во всем мире с дефектами конечностей. Эффект талидомида как снотворного был обнаружен в 1962 году. До этого, выпуск на рынок нового препарата рассматривался без сильного опасения. История с талидомидом вынудило фармацевтические компании тщательно тестировать лекарства перед выпуском.
Разработка и продажа талидомида
Талидомид был разработан в 1950-х годах на Западе немецкой фармацевтической компании Chemie GmbH Grunenthal, чтобы расширить ассортимент продукции компании, которая до этого специализировалась на антибиотиках. Первоначально планировалось, что это будет лекарство против судорог, но вместо этого у него обнаружились свойства мягкого снотворного. Казалось, что это прекрасная замена модным транквилизаторам.
В процессе патентования и испытания, ученые поняли, что препарат было невозможно передозировать (LD50 уровень). Исследования на животных не включали тесты во время беременности. Казалось бы все в порядке и “безобидный” талидомид получил лицензию в июле 1956 года как мягкое снотворное, отпускаемое без рецепта для продажи в Германии и большинстве европейских стран. Лекарственное средство также уменьшило утреннее недомогание, таким образом, снотворное стало популярным среди беременных женщин.

Первые подозрения и несчастия
К 1960 году врачи были обеспокоены возможными побочными эффектами. У некоторых пациентов было обнаружено повреждение нервов в конечностях после длительного использования талидомида. Grunenthal не представила убедительных клинических доказательств, опровергающих существования проблем. В Соединенных Штатах Управление по контролю за продуктами и лекарствами (FDA) и ревизор лекарственного средства Фрэнсис Олдхэм Келси не одобрил талидомид для использования.
Было обнаружено увеличение рождений пораженных талидомидом детей в Германии и в других местах. Однако связь с талидомидом не была официально установлена до 1961. Снотворное было изъято с рынка только после исследований и предложения существования связей между приемом талидомида и повреждением конечностей, немца Видукинда Ленца и австралийца Уильяма Макбрайда независимо друг от друга. Более чем 10 000 детей во всем мире родились с поражениями конечностей по причине према матерями во время беременности этого препарата. Среди известных людей в Великобритании актер и автор Мэт Фрейзер получил проблемы вызванные талидомидом.

Последствия и спорное возвращение во врачебную практику талидомида
Проблемы с талидомидом породили долгий уголовный процесс в Германии и громкую компанию в британских газетах. Они вынудили Grunenthal и ее британсого представителя, имеющее патент на деятельность в британии, Distillers Company, заставить выплачивать компенсации пострадавшим от этого лекарства. Случай с талидомидом повлек более жесткое тестирование и выход лекарств на рынок во многих странах, включая Соединенные Штаты и Соединенное Королевство.
В 1964 больному лепрой в госпитале университета Иерусалима Хаддасах дали талидомид, потому что другие транквилизаторы и болеутоляющие не действовали. Израильский доктор Джейкоб Шескин заметил, что лекарственное средство также уменьшило симптомы лепры. Исследование относительно эффектов талидомида на лепру заканчилось Всемирной организацией здравоохранения (ВОЗ) в 1967 году серией клинических испытаний. Положительные результаты талидомида против против лепры подтвердились во многих развивающихся странах. Его также используется успешно, чтобы управлять некоторыми связанными со СПИДом последствия. Его эффект при различных формах рака исследуются.
Использование талидомида остается спорным. Положительное влияние при лечение лепры неоспоримо. Однако, существует риск новых пострадавших при рождение от талидомида, особенно в странах, где контроль не может быть эффективным. Черный рынок также может преподнести ряд сюрпризов.
Меню раздела